Arnaldo Carlos Caponetti: Clínica San Camilo. Ciudad de Buenos Aires.
Dirección Postal: Segurola 170, Buenos Aires (1407).
E-mail: capo47@hotmail.com
Introducción
Un hecho habitual en la práctica diaria es la consulta por parte de los pacientes acerca de la posibilidad de despertar durante la cirugía o tener dolor durante un procedimiento. Dicho temor puede ser motivo de ansiedad manifiesta para la mayoría de los pacientes. Puede denominarse como “estado de inconciencia parcial” (EIP) y se define como la capacidad que tiene un paciente de recordar en forma espontánea o inducida cualquier evento acontecido entre la inducción y la recuperación de la conciencia al final de la cirugía1-3.
Esa ansiedad ha sido a veces potenciada por relatos de otros pacientes, que se entremezclan con algunos de los mitos acerca de los procedimientos anestésicos utilizados.
La posibilidad de que tales hechos sucedan es conocida desde que se ha generalizado la utilización de relajantes musculares por Griffith y Johnson desde 1942 en adelante4; si bien la perspectiva histórica muestra que ya en 1845 Horacio Wells no pudo demostrar las propiedades anestésicas del óxido nitroso y un año más tarde William Morton tuvo éxito al anestesiar con éter dietílico a su paciente (Gilbert Abbot) en el mismo lugar, el Massachusetts General Hospital. En este último caso, el paciente refirió haber estado despierto, pero sin dolor durante la cirugía.
Para poder evaluar las distintas percepciones que puede tener un paciente, se debe diferenciar la memoria explícita, que es la referida a la recolección conciente de eventos ocurridos, de la memoria implícita, que se refiere a cambios en la conducta o razonamiento producidos por experiencias previas sin que se tenga memoria de ellos (el paciente no conoce lo que él sabe)5,6.
El fenómeno puede escalonarse en cuatro estadíos, a medida que se va profundizando la anestesia7 :
- Percepción conciente con memoria explícita.
- Percepción conciente sin memoria explícita.
- Percepción subconciente con memoria implícita.
- Ausencia de percepción.
Un paciente relajado, que se encuentra en el estadio 4, no tendrá memoria explícita o implícita de ningún suceso intraoperatorio; mientras que si se hallara en el estadio 1, nos encontraríamos ante una falla grave en el suministro de anestésicos.
Mientras que el fenómeno de memoria implícita es un proceso normal en pacientes totalmente despiertos, no está claro aún si este proceso puede ser más resistente a los efectos de los anestésicos que los involucrados en la memoria explícita. Además, al aumentar la edad se deteriora tanto una como otra; aunque dicho deterioro sería menor respecto de la memoria implícita, por lo que los hallazgos que relacionan menor edad y mayor ansiedad con más posibilidades de tener memoria implícita son coherentes con los hallazgos estadísticos encontrados8.
Cuando se habla de conciencia intraoperatoria se deben distinguir dos conceptos diferentes:
- Insuficiente anestesia.
- Recuperación de la conciencia en planos quirúrgicos aparentemente adecuados.
El primer caso reseñado con detalles y publicado fue el de Winterbottom (1950), quien lo describe como de insuficiente anestesia —paciente ventilado con oxígeno únicamente, cerca de una hora— por conocimiento insuficiente en el uso de los relajantes musculares9.
Lo que no se halla en duda es que la concentración de anestésicos generales requeridos para abolir la conciencia y la memoria explícita, de un evento intraoperatorio, es mucho menor que la requerida para abolir movimientos en respuesta a estímulos dolorosos10.
Desafortunadamente, este punto y el concepto de CAM han “fijado” el razonamiento en anestesia por 30 años y es momento de reconsiderar otros elementos relacionados con la acción de los anestésicos y su efecto sobre la función cognitiva11.
La anestesia general no es un “fenómeno de todo o nada” y, a medida que se profundiza, la conciencia y memoria explícita representan sólo una parte de un espectro más amplio de la función cognitiva.
En 1955, Artusio demostró que durante cirugía cardíaca y abdominal pudo tener pacientes concientes, cooperativos y sin dolor utilizando éter en planos anestésicos superficiales, sin recuerdo explícito de lo sucedido en el postope-ratorio12.
Diez años después, Levinson estudió diez voluntarios durante cirugía dental con anestesia general, a los que sorprendió en la mitad del procedimiento con una exclamación acerca del color de sus mucosas por una supuesta falta de oxigenación (“crisis inventada”). Si bien en el postoperatorio no tuvieron recuerdo explícito de lo expresado, un mes más tarde y bajo hipnosis, cuatro de ellos recordaron con fidelidad lo acontecido, mientras que otros cuatro tuvieron recuerdos parciales.
Este estudio demuestra que los pacientes pueden retener la habilidad para procesar información auditiva, aun estando suficientemente anestesiados para permanecer sin respuesta a la estimulación quirúrgica (y sin que haya recuerdo explícito)13,14.
Los dos mayores conceptos relativos a memoria y despertar, clásicamente aceptados, son que durante la anestesia hay un momento “umbral” por arriba del cual hay recuerdo de los hechos y debajo del mismo no queda memoria de los mismos. El segundo concepto es que el despertar conciente es sólo la punta de un iceberg, ya que durante (en apariencia) adecuados planos quirúrgicos el proceso de información asociado con funciones superiores como comprensión del lenguaje y reconocimiento continúa, pero sin recuerdo conciente15.
Incidencia
La incidencia de despertar con las técnicas utilizadas habitualmente ha sido reportada en Estados Unidos de un 0,2 a 0,4% en pacientes con cirugía no obstétrica ni cardíaca, siendo de un 0,4% en cesáreas y hasta de un 1,5% en cirugía cardíaca. La incidencia es aun mayor en los centros de trauma con pacientes en estado crítico y de alta complejidad (11 al 43%)16.
En ese país, donde se administran aproximadamente 25 millones de anestesias al año, se estima que unos 40.000 pacientes experimentan algún grado de despertar intraoperatorio durante ese período17.
Al igual que en nuestro medio, el hecho de que no se consignen la mayor parte de los mismos hace que no aparezcan como dato estadístico.
En el estudio de Karen Domino (ASA Closed Claim Project), las demandas por despertar intraoperatorio fueron un 1,9% sobre el total de las estudiadas, en un porcentaje similar a quemaduras, neumonía aspirativa e infarto de miocardio18.
Comparado con otros reclamos, la mayor parte fue efectuada por mujeres (un 77% vs. 59% de otros daños), en pacientes de menos de 60 años de edad (en 89% de los casos vs. 79% de otras causas) y en cirugías electivas (87% de las demandas vs. 72% de otras causas). La severidad del daño causado fue menor que para otros incidentes anestésicos, con un 95% de injuria de carácter temporal. La mayor cantidad de mujeres involucradas puede deberse a los casos obstétricos que aumentan la incidencia sobre los totales.
En el mismo estudio, se hace una distribución de las demandas según la década de aparición. La distribución temporal muestra que los reclamos han venido aumentando desde 1970 hasta la actualidad. Esto se relaciona con una mayor difusión pública del fenómeno en diversos medios antes que a un aumento en su incidencia, lo que lleva a los pacientes a denunciarlo, cuando anteriormente era habitual, por pudor, ocultarlo19.
En un estudio de Hargrove del año 1987, se describe en porcentuales una distribución de las causas de EIP según su origen. De acuerdo al mismo, se puede observar que los errores de técnica anestésica son la causa de mayor incidencia, pudiendo incluirse dentro de dicho grupo las fallas en la revisión de circuitos y/o en el equipamiento20 (ver Figura 1).
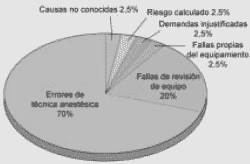 [ Ampliar imagen ] |
| Figura 1: Causas de EIP durante anestesia, según un estudio de Hargrove20 |
Clasificación de los incidentes
- Paciente relajado y despierto: ocurre en el período de preinducción e inducción; los de más alta vulnerabilidad, generalmente, por error en el suministro de drogas, por falta de rótulo o identificación de las jeringas (generalmente succinilcolina u otro relajante en lugar de morfinosí-miles, benzodiacepinas o hipnóticos)21,22. También puede incluirse en este grupo a los pacientes con intubación dificultosa, en quienes los reiterados intentos no van acompañados de dosis supletorias de hipnóticos.
- Paciente despierto durante el período de mantenimiento: es el que luego detalla haber escuchado sonidos y comentarios, generalmente referidos a su aspecto físico o peso corporal, o, peor aún, haciendo una prognosis negativa de la evolución de su enfermedad18
Consecuencias
El despertar durante el transcurso de una anestesia general es una experiencia que asusta al paciente y puede ocasionarle una seria injuria emocional e, inclusive, un desorden comparable al estrés postraumático. Los pacientes que experimentaron despertar con recuerdo explícito describen sobre todo percepción auditiva con sensación de parálisis, ansiedad, pánico e imposibilidad de pedir ayuda; además de la sensación de que algo equivocado está sucediendo y nadie lo percibe15,23 .
La sensación de dolor ocurre menos frecuentemente (aproximadamente en un 10% de los pacientes con despertar); aunque, si está presente, empeora la vivencia y su posterior evolución. Sin duda el dolor es la mayor fuente de estrés durante el despertar intraoperatorio o al finalizar la cirugía4.
Más del 70% de los pacientes con conciencia y recuerdo tuvieron en el período postoperatorio sensaciones desagradables con pesadillas, ansiedad, irritabilidad y preocupación exagerada con vivencias relacionadas con su propia muerte. Es frecuente el temor de que pueda volver a sucederle algo similar en otra intervención, y ello lo aleja de las consultas médicas en general24 .
Los pacientes son reacios a relatar los trastornos en su personalidad, si ya tenían patologías previas de orden psicosomático. Otros factores acompañantes son la respuesta emocional a la enfermedad y al motivo de la cirugía.
Respecto a las compensaciones económicas, hay variabilidad entre los distintos países, siendo la media de u$s18.000 y llegando la más onerosa a u$s 600.000.17
Secuelas emocionales y recuerdo durante anestesia general
En el análisis de la Dra. Domino18 (ver Tabla I) se destaca el hecho de que los pacientes que reclamaron por despertar, en muchos casos, no mostraron los signos clásicos, como hipertensión y taquicardia, que habitualmente han sido utilizados como indicadores del plano anestésico y, aunque actualmente se les considere como predictores pobres del nivel de sensorio, no deben ser descartados15,25.
| TABLA I Secuelas emocionales y recuerdo durante anestesia general18. | |||
| Eventos Intraoperatorios | Secuelas Postoperatorias | ||
| Sonidos | 30% | Distrés emocional temporario | 84% |
| Sensaciones táctiles sin dolor | 25% | Pesadillas recurrentes | 16% |
| Dolor | 21% | Necesidad de psicoterapia | 13% |
| Parálisis | 20% | Estrés postraumático | 10% |
| Intubación | 15% | ||
| Pánico | 11% | ||
No menciona otros signos físicos como sudoración, lagrimeo o expresión facial (muecas, ceño fruncido, cambios en el tono de los músculos de la cara). Sólo un paciente tuvo movimientos, puesto que los otros se hallaban relajados.
Pacientes tratados con bloqueantes beta o de los canales de calcio, opioides u otras drogas con propiedades vagotónicas, reducen la sensibilidad de sus barorreceptores, llevando a enlentecer la frecuencia cardíaca, lo que puede enmascarar alguna de las respuestas autonómicas26.
La detección de memoria explícita o recuerdo de hechos intraoperatorios es sencilla y puede hacerse en base a pocas preguntas, preferentemente luego del regreso del paciente a la sala y transcurridas algunas horas desde el final de la intervención27.
Cuestionario sugerido para detectar estado de inconciencia parcial
- żQué es lo último que recuerda previo a dormirse?
- żQué es lo primero que recuerda después de la cirugía?
- żPuede recordar algo entre esos dos momentos?
- żTuvo sueños durante la cirugía?
- żQué fue lo más desagradable de su experiencia quirúrgica?
La referencia a los sueños y la posibilidad de recordarlos se relaciona con niveles superficiales de anestesia, si bien muchos pacientes que tuvieron recuerdo de hechos intraoperatorios son reacios a contar sus experiencias. Los sueños se clasificaron como agradables, neutros o desagradables, de acuerdo al contenido emocional de los mismos. Estos últimos son considerados en algunos estudios como relacionados con posibles estados de inconciencia parcial.28
Un trabajo de Nordstrom en Suecia, basado en tres entrevistas: la primera, en sala de recuperación, y las otras dos en los días subsiguientes, identifica un caso de estado de inconciencia parcial con desarrollo de neurosis postrau-mática al cuarto día de la cirugía, sin otros recuerdos del período intra y perioperatorio en una anestesia efectuada con isoflurano.
En algunos pacientes surgen recuerdos hasta 8 días después, con detalles vívidos que no se habían manifestado durante el postoperatorio inmediato. En contraste con este hecho, surgen casos que relatan despertar intraquirúrgico en la sala de recuperación y niegan tener recuerdo alguno al día siguiente2 9. La detección es importante, pues se puede evitar el desarrollo del síndrome de estrés postraumático que ocurre en el 10% de los casos. En ocasiones, la empatía con el anestesiólogo y comprensión del hecho por sí solos evitan consecuencias posteriores –una explicación detallada y creíble limita el daño, permitiendo al paciente recuperar la confianza en sus médicos30.
En casos de experimentación clínica, se efectuaron tests psicológicos e hipnosis, pudiéndose recolectar datos guardados en la memoria que no llegaron a hacerse concientes30.
Estudios recientes, efectuados en un centro de trauma, demostraron que tanto la memoria implícita como la explícita disminuyen a medida que la profundidad anestésica aumenta31.
También se hicieron experiencias, estando los pacientes en planos quirúrgicos habituales, con sugestiones verbales acerca de determinados comportamientos. Los resultados fueron positivos para mostrar signos de memoria implícita. De ello surge como importante la influencia que pueden tener, en un sentido o en otro, los comentarios que se hacen acerca del resultado de la intervención (sugestión positiva)32.
Para que los fenómenos relacionados con la posibilidad de mantener la conciencia y su recuerdo sean mejor comprendidos, la siguiente sinopsis relaciona el concepto de “plano” anestésico y cantidad de agente administrado.
żA qué se llama profundidad o plano de anestesia?
En el curso de la práctica habitual muchas drogas anestésicas son utilizadas según dosis estandarizadas y sin aplicación de los conocimientos farmacocinéticos y dinámicos para controlar su utilización. Estos esquemas se basan en la premisa “se administra equis cantidad de una droga y se observa al paciente para ver qué pasa“; cuando en realidad lo que se debiera conocer es la concentración plasmática de la droga en cuestión y, mejor aún, la concentración en el lugar de efecto (SNC). Allí, la cantidad de droga presente no es mensurable, aunque sí es posible su estimación.
En estos parámetros se basan los sistemas TCI (Target Controlled Infusion) en los que se extrapolan datos de miles de pacientes; esa información se adecua a los parámetros que se ingresan en la bomba de infusión, en el caso del empleo de anestesia intravenosa33.
En el caso de anestesia inhalatoria, la concentración tidal expirada del agente utilizado es el indicador más fiable para evaluar la dosificación de ésta34.
La CAM, como concepto, fue desarrollada por Eger (1965) y lleva a la noción de que la prevención de respuestas somáticas a un estímulo nocivo es parte de un efecto continuo por parte de los anestésicos generales. Eger define la CAM como la concentración alveolar mínima requerida para abolir movimientos en respuesta a estímulos quirúrgicos en el 50% de los pacientes35.
Para poder incorporar la abolición de reflejos nociceptivos a la noción de anestesia general, se debe aceptar el concepto de CAM-BAR que es la concentración de agente anestésico necesaria para prevenir la respuesta autonómica en el 50% de los pacientes, con un valor mayor que la definida por Eger.
Con la evolución del conocimiento acerca de los anestésicos generales, hoy se reconocen la CAM-despertar y la CAM-sueño, que suponen dosis menores a la CAM de Eger para abolir procesos cognitivos. Es probable que, en base a esa idea, se hayan estado sobredosificando numerosos pacientes en los últimos treinta años. Las curvas de CAM se ubican de menor a mayor en el siguiente orden: CAM-despertar, CAM-incisión, CAM-intubación, CAM-BAR. Se puede observar que la intubación aparece como un estímulo nocivo más fuerte que las noxas de origen quirúrgico. Para éstas, las curvas CAM se ubican entre CAM-incisión y CAM-intubación11.
Así, hoy en día, se debe enfatizar el concepto de que los anestésicos generales producen abolición de la conciencia antes que abolición de la respuesta a los estímulos quirúrgicos11.
También para agentes intravenosos han sido medidas las concentraciones en sangre para niveles correspondientes a Ce (Concentración efectiva) homólogas a las anteriores: Ce50-despertar y Ce50-sueño. Los valores de la tabla II muestran que la abolición de conciencia ocurre a un 50 %, aproximadamente y de acuerdo al agente, de la dosis requerida para evitar movimientos como respuesta a estímulo nocivo (CAM-Eger)11.
| TABLA II Relaciones entre CAM-despertar/CAM-Eger para diferentes anestésicos. | |||
| CAMdespertar% | CAMEger% | Relación CAMdespertar/CAM | |
| Halotano | 0,40% | 0,74% | 55% |
| Isoflurano | 0,50% | 1,28% | 39% |
| Desflurano | 2,50% | 5,00% | 50% |
| Sevoflurano | 0,70% | 1,70% | 41% |
| Propofol (µ/ml) | 3,40-4,30% | 8,10-12,20% | 40% |
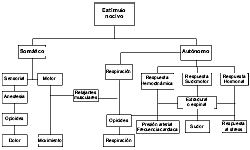
En la figura 2 se observa, de izquierda a derecha, cómo las respuestas a estímulos nocivos son suprimidas por opioi-des o anestésicos generales.
 [ Ampliar imagen ] |
| Figura 2: Efectos de los estímulos nocivos y supresión de respuestas a los mismos.36 (modificado) |
Con relación a la respuesta del sistema autónomo al estímulo quirúrgico, en estudios recientes37, se demostró que el isoflurano administrado a altas concentraciones (2 CAM) no previene las respuestas autónomas desde el comienzo y hasta el final de la cirugía.
Esto implica que los volátiles solos se hallan limitados en su acción y varían en su capacidad para suprimir la respuesta autonómica que, de por sí, es uno de los componentes de la definición de anestesia36. Existe una extendida creencia de que la supresión de respuestas simpáticas al estímulo quirúrgico asegura un plano suficiente para mantener inconciencia. Esta creencia es reforzada porque, en general, las concentraciones anestésicas necesarias para abolir respuestas autonómicas son mayores que para mantener al paciente inconciente. Esto puede no ser cierto para todos los pacientes. Algunos pueden estar completamente despiertos y concientes de hechos intraoperatorios y no presentar cambios hemodinámicos o aumento de actividad simpática62. A la inversa, las respuestas hemodinámicas o somáticas no se relacionan, necesariamente, con recuerdo o recuperación de la conciencia.
De igual manera, el propofol por sí sólo no puede abolir respuestas autonómicas a la incisión en piel, pero si se le adiciona fentanilo u otros opioides en una concentración efectiva, sí lo hace, aún a bajas concentraciones38,39. Los opioides, por su parte, anulan la respuesta a la estimulación quirúrgica antes de producir hipnosis40.
Hay evidencia creciente de que los agentes volátiles actúan dentro de una porción identificable de una proteína de la membrana celular bilipídica. Se han encontrado sitios de unión para los agentes volátiles en el receptor GABA, lo que implica un modo de acción más específico.
La mayoría de los agentes intravenosos se unen también al receptor GABA, en tanto que los opioides se unen al receptor morfínico específico41.
Las experiencias en laboratorio indican que los anestésicos generales previenen la respuesta ante un estímulo nocivo debido a su acción sobre la médula espinal y no por su acción sobre el nivel supraespinal del SNC.
Los agentes volátiles tienen una acción dual: pérdida de conciencia a bajas concentraciones, por una acción supraespinal, e inhibición de la transmisión nociceptiva a nivel medular. No hay para los agentes volátiles un mecanismo unitario ni un lugar único de acción, sino múltiples sitios de acción. También se ha demostrado para agentes intra-venosos como el propofol y el tiopental que las concentraciones necesarias para inhibir las respuestas son hasta cuatro veces mayores que para producir pérdida del sensorio.
Además, si utilizamos opioides dentro del rango analgésico, bastan dosis bajas para reducir la CAM de los halogenados y la Ce de los agentes intravenosos. Al aumentar la concentración se observa que, tanto para agentes inhalatorios como endovenosos, se llega a un efecto ”techo“.
El resultado de los estudios realizados indica que para prevenir una determinada respuesta autonómica a un estímulo nocivo, se requiere una efectiva analgesia combinada con una concentración suficiente del anestésico volátil o IV como para producir pérdida de conciencia
Hay al menos dos componentes en el estado anestésico:
- Pérdida de conciencia y recuerdo: imposibilidad de responder o recordar un estímulo no nocivo.
- Anular las respuestas a estímulos nocivos.
Se puntualiza que puede alcanzarse un nivel, sin tener seguridad de que se alcanzó el otro40.
En un lejano (1987) pero aún vigente editorial, Prys-Roberts36 enfatiza que la analgesia, relajación muscular y supresión de la actividad autonómicas son efectos farmacológicos que pueden ser alcanzados en forma individual por drogas específicas. Mientras que algunos agentes inhalatorios o intravenosos (incluyendo los opioides) pueden ejercer algunos o todos esos efectos en mayor o menor grado, la supresión de la percepción sensorial es el único rasgo en común que tienen todos los anestésicos generales.
Así, considera a la anestesia como el estado que asegura la supresión de los componentes sensoriales somáticos y viscerales y la percepción del dolor. Analgesia, relajación muscular y supresión de la actividad autónoma no son componentes de la anestesia, sino que deben ser considerados como suplementos deseables del estado de anestesia que hacen posible la cirugía.
También Kissin39,40, en términos parecidos, analiza y redefine a la anestesia como un amplio espectro de acciones farmacológicas que, por vía de las distintas drogas utilizadas, crean el estado de anestesia general. El espectro de efectos que constituyen ese estado no debe ser considerado como la suma de varios componentes, sino como la suma de acciones farmacológicas distintas, aun si la anestesia es producida por una sola droga (Tabla III).
| TABLA III Definiciones del Estado de Anestesia40 | |
| Autores | Definición |
| Prys-Roberts | Supresión de la percepción sensorial producida por drogas en la que el paciente no percibe ni recuerda el estímulo producido por noxas quirúrgicas. |
| Eger | Inconciencia-olvido e inmovilidad. |
| Pinsker | Parálisis, inconciencia y atenuación de respuestas al estrés. |
| Woodridge | Bloqueo sensorial, bloqueo motor, blo-queo de los reflejos y bloqueo mental. |
| Kissin y Gelman | Todos efectos separados para proteger al paciente del trauma quirúrgico. |
Hipótesis de P. Glass para explicar el proceso de anestesia general
Para una mejor comprensión de los fenómenos relacionados con los estados de vigilia y sueño, puede resultar de utilidad la teoría de Peter Glass respecto a la posibilidad de la existencia de centros específicos del SNC relacionados con la conciencia. En un reciente editorial42,43 señala que la interacción entre hipnóticos y opioides, para alcanzar los dos mayores objetivos de la anestesia general (pérdida de conciencia e inhibición de la respuesta al dolor), está basada en que ambos no son parte de un continuo o más profundo “plano“ anestésico, sino dos fenómenos distintos, producto de la estimulación de diferentes centros en el SNC y médula espinal.
La teorización de Glass propone, respecto a los procesos que llevan al estado de anestesia general, que dentro de centros superiores del cerebro existiría uno que es responsable desde el aumento de sedación hasta la pérdida de conciencia. Este centro estaría activado por todas las entradas sensoriales al cerebro. Lo inhibirían anestésicos, hipnóticos y sedantes que, con suficiente concentración, producen pérdida de conciencia. Puede ser activado por estímulos que provoquen estrés e incrementen la actividad autonómica o que aumenten las catecolaminas circulantes. También, una mayor estimulación sensorial de la conciencia puede por sí misma aumentar la actividad autonómica.
Por todo lo anterior, los diversos estados de conciencia (con o sin sedación o pérdida del sensorio) son la resultante de un efecto neto de estimulación versus concentración de drogas sedantes.
No todos los estímulos activan a este centro por igual (la intensidad y el tipo de estímulo son importantes); por ejemplo, los estímulos dolorosos quirúrgicos son activadores del centro de la conciencia, de ahí que un paciente pueda no responder a un estímulo no nociceptivo débil y sí hacerlo ante uno doloroso.
La inhibición del estímulo nociceptivo se produce a nivel de la médula espinal por opiáceos en dosis suficientes o por agentes volátiles a mayores concentraciones que las requeridas para pérdida de la conciencia44-45. Los anestésicos locales también producen esa inhibición en nervios periféricos, plexos nerviosos o médula espinal.
La anestesia general es un proceso en el cual el cerebro permanece inconsciente por drogas sedantes o hipnóticas y la transmisión del estímulo nociceptivo es inhibida a nivel medular o inframedular (plexos o troncos nerviosos), no pudiendo alcanzar estructuras superiores (cerebro) y alterar el estado del sensorio.
El concepto de plano anestésico debe ser revisado para que refleje los componentes en forma individual; sólo así se podrán evitar en forma racional los fenómenos de incon-ciencia parcial.
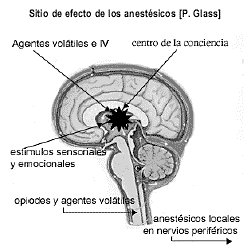
Como se puede observar en la figura 3, Glass separa la pérdida de la conciencia y respuesta al dolor refiriéndoles distintos lugares anatómicos dentro del sistema nervioso e interrelaciones entre sí.
 [ Ampliar imagen ] |
| Figura 3: Hipótesis acerca del sitio de efecto de los anestésicos (P.Glass). |
Cómo medir el estado o profundidad del plano anestésico
Una primera consideración a tener en cuenta es que resulta difícil cuantificar algo que todavía no se halla bien definido, tal como “plano” anestésico.
Comprender al estado de anestesia general como una combinación de diferentes componentes, alcanzado a través del uso combinado de drogas con distintos mecanismos de acción, tiene una profunda relevancia cuando se debe mensurar la profundidad de la anestesia, ya que diferentes componentes de ese estado de anestesia debieran ser determinados específicamente para varias combinaciones de esas drogas. Utilizar esas combinaciones hace que la búsqueda de un indicador fiable de profundidad anestésica se transforme en la búsqueda de diferentes índices para los distintos componentes de ese estado40.
Cuando no se cuenta con otros parámetros, habitualmente se utilizan las respuestas hemodinámicas del paciente para juzgar el “plano” anestésico y ajustar dosis. Las bases científicas para actuar de esta forma no son claras, ya que esas variables pueden ser modificadas por distintas patologías, drogas y técnicas quirúrgicas.
Los opioides hacen aun más difícil establecer la profundidad de la anestesia, debido a que suministrados en altas dosis pueden producir un estado clínicamente no distinguible del inducido por agentes volátiles o intravenosos, aunque a esas dosis causen supresión de la ventilación36.
Las siguientes son una serie de técnicas que se han propuesto para medir la profundidad anestésica46 (ver Tabla IV).
| TABLA IV Métodos para detectar adecuado plano anestésico.57 modificado | ||
| Método | Ventajas | Desventajas |
| Signología clínica | ||
| Despertar. Movimientos. | Es el signo a buscar. Obvio y fidedigno. | Es retrospectivo. Puede ocurrir sin recuerdo. No es útil si usamos relajantes. |
| Frecuencia y patrón respiratorio.Signos Autonómicos (FC-TA-pupilas-sudor). Altamente no específicos. | Moderadamente confiable. Disponibles y muy utilizados. | No es útil si usamos relajantes. Poco confiables. |
| EEG | ||
| Señal “cruda”. | Relativamente fácil de monitorear. | Difícil de interpretar. No independiente del agente. |
| Señal procesada simple (SEF). | Más fácil de interpretar. | Necesita equipo especial. No independiente del agente. No muy confiable. |
| Señal procesada compleja (BIS). | Fácil de interpretar.Muy confiable. | Necesita equipo especial. Necesita mayor evaluación. |
| Otras técnicas | ||
| Músculos faciales. | No afectados por relajantes. | Necesita equipo especial. Necesita mayor evaluación. |
| Contractilidad del esófago. | Ninguna ventaja aparente. | Necesita equipo especial. No específico y no confiable. |
| Potenciales evocados. | El más útil en dormido/despierto. | Necesita mayor evaluación. Necesita equipo especial. |
| Microtemblor ocular. | Probado sólo con propofol. | Necesita mayor evaluación. |
| VFC-ASR. | Predictor de inadecuada analgesia. | Necesita mayor evaluación. |
Técnica del brazo aislado (BA)
En ésta, un brazo es excluido de la circulación con un torniquete, permitiendo la respuesta muscular al no estar relajado. Está limitada por el tiempo en que puede mantenerse el torniquete y por que sólo indica si el paciente se halla despierto o dormido, sin evaluar el plano anestésico.
Frecuencia de contracciones del 1/3 inferior del esófago (FCE)
En la práctica clínica, por inconsistencia en sus registros, ha dejado de utilizarse47.
Variabilidad de la frecuencia cardíaca (VFC)
Los componentes de alta frecuencia del denominado VFC, se relacionan con la arritmia sinusal respiratoria (ASR) y son estimados por los intervalos RR en el ECG. Se describe una reducción en la variabilidad de la arritmia sinusal respiratoria según se incrementa el plano de profundidad anestésica, de acuerdo a una técnica denominada polinomial. Si bien hay escasa experiencia con el método, existen dos equipos en venta denominados “Fathon”® y “Anemon”® que utilizan dicho principio. El recurso es invalidado en presencia de neuropatía diabética y fibrilación auricular48-50.
Varias hipótesis explican cómo la anestesia disminuye la ASR. El mecanismo implica la estimulación de las sinapsis inhibitorias glicinérgicas y GABAérgicas en el eje Núcleo del Tracto Solitario-Núcleo Ambiguo. Sus proyecciones inhiben centros superiores en el cerebro, como el sistema límbico, modulando así los anestésicos el nivel de péptidos hipotalámicos endógenos responsables del metabolismo cerebral e influyendo sobre el control vagal del ritmo cardíaco. De esta manera, la reducción del metabolismo cerebral se relaciona con las variaciones del mismo51.
Tomografía de emisión de positrones (TEP)
La TEP proporciona una imagen funcional del cerebro que permite analizar los diferentes equipos utilizados para medir la profundidad o plano anestésico. Durante la anestesia con propofol e isoflurano, muestra disminución en el metabolismo de glucosa o, lo que es lo mismo, menor metabolismo cerebral que se correlacionan linealmente con reducciones en el análisis biespectral (BIS) y con la ASR; pero no con los potenciales evocados auditivos de potencia mediana (PEAPM). Esa reducción del metabolismo es un componente importante del plano anestésico. Los estudios efectuados llevarían a la hipótesis de que los agentes anestésicos pueden interferir con los procesos de regulación del metabolismo cerebral, de manera similar al proceso de hibernación de algunos mamíferos. Muchos rasgos de ésta son parecidos al estado anestésico, tales como ondas delta en el EEG, pérdida de termorregulación, respuesta lenta al estímulo y falta de función cognitiva. De este modo, la anestesia podría ser desencadenante de un mecanismo de hibernación latente en el hombre y otros mamíferos48.
Electromiograma espontáneo de superficie (EES)
En pacientes no paralizados por relajantes, el EES es registrado desde varios grupos musculares. Se utilizan los músculos del abdomen, cara y cuello. Los músculos faciales son más resistentes que otros músculos periféricos a los relajantes, pudiendo mensurarse voltajes desde el frontal, zigomático, orbicular y otros músculos oculares utilizando electromiografía con electrodos cutáneos. Ello sugiere que el patrón de tensión muscular (mueca o sonrisa) puede indicar plano anestésico adecuado. Dado que esta información es imprecisa, tienen poca utilidad clínica.
Electroencefalograma (EEG)
Su interpretación requiere por lo general un neurólogo o neurofisiólogo. Aquí, la informatización del EEG toma relevancia y se hace útil para su uso en cirugía y terapia intensiva.
El EEG “crudo” se descompone en varias ondas sinoidales que tienen relaciones temporales y de fase unas con otras. Éste se procesa convirtiendo secciones cortas (llamadas “epochs” de 2 a 30 seg.) en ondas digitales, que son sometidas a una compleja manipulación matemática conocida como Fast Fourier Transformation (FTT), que separa las señales del EEG en ondas sinoidales. Cada una tiene diferente amplitud; pero la suma de todas contiene al EEG original.
Cada epoch (segmento procesado) puede ser mostrado en forma gráfica; y muchos de ellos, unos arriba de otros, producen un patrón típico con picos y valles llamado compresión espectral.
Los picos representan las frecuencias donde se localizan las de mayor amplitud o poder. Se calculan las frecuencias debajo de las cuales encontramos un 95% del total de las de mayor amplitud o poder, conocidas como Spectral Edge Frecuency (SEF), que tienen la ventaja de ser un número simple que se correlaciona con la profundidad de anestesia.
Este análisis del poder espectral del EEG no contiene las relaciones entre las distintas fases del mismo, lo que sí consigue el análisis biespectral. Este análisis, denominado BIS, es un parámetro del EEG digitalizado que varía desde rango 0 (EEG plano), para un nivel de muy profunda anestesia, hasta 97-100, si el paciente está despierto. El BIS es utilizado para determinar las relaciones de fase de los componentes fundamentales del EEG. Fisiológicamente, estas relaciones de fase corresponden al grado con que las células nerviosas que generan el EEG actúan sincrónica o caóticamente. El EEG del estado despierto es predominantemente de baja amplitud y alta frecuencia. Los agentes anestésicos alteran este patrón y lo transforman en uno de mayor amplitud y menor frecuencia.
Si ese fuera el único efecto de los anestésicos y si el cambio en amplitud y frecuencia fuera lineal al aumento en la dosis, la correlación entre EEG y el efecto de la droga sería muy simple; pero hay otros efectos de los anestésicos difíciles de cuantificar que pueden modificar los valores del BIS, aunque permiten seguir la tendencia en la escala 0 a 100.
Un valor de BIS por debajo de 50-60 se asocia con muy baja probabilidad de respuesta a órdenes verbales. El umbral de recuerdo es más alto, con bajas posibilidades de recordar a valores menores de 70. Asimismo, puede predecir respuestas tales como movimientos luego de incisión en piel durante anestesia, con distintos agentes utilizados en combinación o no52,53.
La utilidad del BIS ha sido ampliamente comprobada y el correlato con la clínica es muy cercano con propofol, midazolam, tiopental, isoflurano, sevoflurano, óxido nitroso, etomidato y opioides; no así con ketamina, que produce un patrón de descargas que el dispositivo no analiza con exactitud.
La relación con los efectos de las drogas utilizadas es lineal, excepto para los opioides54-57 y el óxido nitroso, para el cual —según estudios efectuados por Barr y col.— BIS no es sensible58.
El empleo del BIS promueve una utilización más racional de los agentes anestésicos con mayor utilización de opioides y de beta bloqueantes para inhibir respuestas autonómicas nocivas59.
Potenciales evocados (PE)
Un potencial evocado es la respuesta eléctrica del SN a un estímulo sensorial, y puede ser seguido a lo largo de las vías nerviosas. Hay tres tipos de estimulación que pueden utilizarse:
- somatosensorial (eléctrica) de nervios periféricos;
- estimulación auditiva, por click o tonos; y
- estimulación visual, alternando patrones visuales.
Los potenciales evocados son de muy baja amplitud y difíciles de distinguir de las ondas del EEG. Para poder hacerlo, se utilizan estímulos repetitivos que permiten separar la señal que viene del potencial evocado del “ruido” de fondo, que corresponde a la actividad cerebral. Los potenciales evocados somatosensoriales se usan para monitorear la médula espinal durante procedimientos que puedan producir isquemia o lesiones.
Los PE auditivos (PEA) más utilizados son los denominados de Latencia Mediana (PEALM) que permiten discernir cambios en amplitud y latencia de las ondas, según se aumenten las dosis de anestésicos. Inversamente, cuando comienza la estimulación quirúrgica, vuelven al estadio anterior (balance entre depresión cognitiva y estímulo quirúrgico)60. Se ha demostrado correlación entre preservación de PEALM y memoria implícita para hechos intraoperatorios.
Un estudio de Doi compara cuatro métodos de evaluación de índices electroencefalográficos durante la fase de despertar al final de cirugía, calculando las señales EEG con decrecientes concentraciones de propofol. Se correlacio-naron valores de BIS, EES (Electromiograma espontáneo de superficie), músculos faciales (MF) y potenciales evocados auditivos (PEA). La mejor correlación la tuvo el BIS, siendo pobre para EES y MF. Si bien para PEA los valores no correlacionaron bien, pudo hacerse una buena distinción entre paciente despierto y dormido. También el BIS tuvo en ese estudio mejor relación entre concentraciones de propofol y estado de vigilia del paciente61.
Para otros autores, ambos métodos son fiables; pero los PEA identifican más rápido los cambios de fase despierto-dormido y dormido-despierto46,62-65.
Es de muy reciente aparición como producto comercial, luego de años de uso experimental, un monitor de PEA, denominado “A-line® ” (Alaris Medical System).
Ventajas al utilizar los PEA66-69 :
- Las variables observadas cambian más rápido y son menos influenciadas por electrocauterio.
- Miden el impacto global de la relación noxa/anestesia sobre el SNC en forma más amplia (analizan la actividad cerebral cortical y subcortical). Son totalmente independientes del agente utilizado.
- No dependen de una base de datos interna para realizar cálculos.
- Pueden mostrar indirectamente insuficiente analgesia en pacientes con aceptable nivel de hipnosis. Microtemblor Ocular (MTO)
Es un temblor de alta frecuencia que afecta los ojos en forma habitual. Es causado por estimulación de la musculatura extraocular y se origina en el área óculomotora del cerebro en su formación reticular. Estos núcleos óculomo-tores son afectados por la actividad neuronal desde otras áreas del tallo cerebral. Se cree que los agentes anestésicos que afectan el sistema reticular, también influencian la actividad del MTO. El movimiento rotatorio desplaza la superficie del ojo entre 150 a 2000 nm, y la frecuencia de oscilación es, en promedio, de 84 Hz. Esta frecuencia es afectada por el nivel de conciencia y muestra un descenso según el grado de hipnosis.
Los estudios hechos hasta el presente lo correlacionan con propofol, determinando una pérdida de conciencia a un promedio de 43,81 Hz, a concentraciones plasmáticas de propofol entre 2 y 3 ?g/ml. El nivel de pérdida de conciencia es variable, pero su rango va desde 27 a 55 Hz.
Los aumentos en la frecuencia indican que el paciente se está despertando, habiendo una certera correlación entre MTO y función del tallo cerebral70.
Utilización del BIS como metodología más difundida
Sus creadores adoptaron una filosofía comercial diferente a la de los otros fabricantes de monitores de plano anestésico. Una vez desarrollado y elaborado el software —en máxima confidencialidad—, se trabajó con la ayuda de un grupo de expertos propio sobre una base de datos con registros previos, para determinar el número BIS que correspondía a cada estadio anestésico. Es decir, no hubo investigadores independientes que colaboraran para su desarrollo48. Posteriormente se instaló la necesidad de su utilización en la opinión pública mediante campañas en los medios71-74.
Incorporando el mismo algoritmo de BIS a la ASR, se encontró que éste es un adecuado predictor de insuficiente analgesia y puede detectar estimulación quirúrgica50,51.
No hay razones académicas acerca de por qué no incorporar otras tecnologías tales como PEA, EES o ASR dentro de un algoritmo similar al de BIS. Aunque se enfatiza que tanto PEA como ASR son reflejos fisiológicos y no una construcción estadística dependiente de la última versión de un software.
Si bien tanto ASR, como PEA, EES y otras técnicas no son funcionalmente equivalentes, pueden ser consideradas ventanas separadas que observan el comportamiento del SNC desde distintos puntos de observación48.
Prevención del despertar intraquirúrgico
Hasta tanto las razones del despertar intraoperatorio sean claramente comprendidas y el monitoreo del índice biespectral (BIS) u otros dispositivos (A-line) se conviertan en un estándar de empleo en quirófano, se debe prevenir la ocurrencia del EIP considerando algunas premisas en relación con la técnica anestésica utilizada.
- Utilizar, como premedicación o preinducción, agentes anestésicos con cualidades amnésicas, tales como las benzodiacepinas o la escopolamina (de uso excepcional en nuestro medio).
- Las asociaciones midazolam-propofol y midazolam-tiopental son sinérgicas, posiblemente por distintos mecanismos de acción75.
- Se puede administrar un adicional a la “dosis sueño” durante la inducción, teniendo en cuenta que la laringoscopía e intubación son estímulos muy importantes y potencialmente nocivos.
Se debe evitar fiarse en exceso del potencial amnésico de las benzodiacepinas que pueden dar una falsa sensación de seguridad, cuando su rango de efectividad varía de paciente a paciente, vinculándose éste fenómeno al de la variabilidad interindividual y a la inducción enzimática que provoca su ingesta crónica (hecho ocultado por los pacientes en numerosos casos), o de otras drogas que tengan una vía metabólica similar.
Veselis et al.76 han demostrado desiguales efectos amnésicos del midazolam, propofol, tiopental y fentanilo. El propofol muestra una alta probabilidad de alcanzar los objetivos de amnesia y sedación, mientras que el fentanilo sólo alcanza los de sedación sin ocasionar amnesia. El propofol tiene efectos similares a los del midazolam, con igual sedación en las concentraciones utilizadas.
En pacientes hemodinámicamente inestables, el uso de ketamina o escopolamina dan una certeza absoluta acerca de la amnesia, si bien sus efectos secundarios deberán ser sopesados77.
Es válido el consejo de Hugh para estos pacientes, cuando expresa que, a menos que su supervivencia sea críticamente dependiente de evitar una hipotensión, la prioridad es asegurar la inconciencia78. Cabe, también, destacar la observación de M. Paladino respecto a las interacciones potencialmente peligrosas entre benzodiacepinas y opioides que, por actuar en diferentes receptores, anulan la compensación hemodinámica y agravan la hipotensión, si no se valoran adecuadamente las reducciones en las dosis empleadas al efecto de producir hipnosis. Aquí la sinergia provoca también efectos no deseados79.
La redistribución rápida en el organismo de los agentes inductores actuales puede resultar en dosis insuficientes, sobre todo, si luego de una inducción endovenosa se continúa el mantenimiento con agentes inhalatorios.
Ese período es de alta vulnerabilidad respecto a la posibilidad de despertar; como así también el estadio “crítico” se prolonga, si se utilizan, previo a la intubación, relajantes con un período de latencia largo (ejemplo: pancuronio o d-tubocurarina).
Deben considerarse dosis suplementarias de inductores en casos de intubación dificultosa en los que se prolonga y reitera la laringoscopía80.
La utilización de relajantes musculares debiera estar reservada para efectuar la intubación y, de ser necesarios durante la cirugía; evitar la relajación completa para poder observar respuestas al estímulo17 (movimientos como indicadores básicos de potencial despertar).
Aumentos en la presión arterial y frecuencia cardíaca de más de 30 mmHg o 30 latidos por minuto deben hacer sospechar, en ausencia de otras causas, un plano muy superficial de anestesia; si bien se consideran ambos indicadores con escaso nivel de predicción81.
Si se utilizan agentes volátiles, la mínima concentración tidal debe ser de 0,8 -1 de la CAM para el inhalatorio en uso82,83. De todas maneras, no hay información fehaciente que garantice que una determinada CAM mínima sea suficiente para asegurar el estado de inconciencia.
Es necesario efectuar una meticulosa revisión de la mesa de anestesia antes de su utilización para asegurar que la provisión de agentes anestésicos llegue con seguridad al paciente, evitando fugas y/o desconexiones en los adap-tadores o en los vaporizadores84.
Monitorear, siempre que se tengan los elementos al efecto, las concentraciones exhaladas de agentes volátiles para asegurarse de que el paciente está recibiendo las adecuadas. En la bibliografía, se menciona una demanda por despertar ajustada a un valor de u$s 150.000, como resultado de un vaporizador vacío no detectado en la revisión previa84. Siempre se debe tener en cuenta que lo que importa monitorear es la concentración en el tidal espirado y no la concentración inspirada. En mezclas no hipóxicas, el óxido nitroso sólo, aún a concentraciones del 80%, puede ser insuficiente para garantizar falta de conciencia y debe adicionársele un agente volátil a una CAM de, por lo menos 0,6 a 0,885. Además, debe considerarse que es posible un amplio grado de susceptibilidad al óxido nitroso y, tal como sucede con otros fármacos, puede haber tolerancia cruzada farmacocinética por abuso de alcohol u otras drogas. El citado agente, puede, “per se”, ser causa de alucinaciones y sueños vívidos que se confunden con estados de vigilia86.
Los opioides en dosis convencionales, por sí solos, no son agentes anestésicos (pueden serlo en dosis muy altas; aun sin asegurar amnesia). Una técnica anestésica basada en óxido nitroso/opioides debiera ser suplementada con un agente inhalatorio o con la infusión de una droga endovenosa como propofol o midazolan78.
Se deben considerar como adyuvantes de los agentes volátiles o endovenosos a los agentes alfa-2 agonistas clonidina y dexmedetomidina que interactúan con receptores adrenérgicos alfa-2 pre y postsinápticos, causando depresión en la función de locus coeruleus (principal núcleo adrenérgico del cerebro87). Los efectos de estos agentes sobre la profundidad anestésica son difíciles de mensurar en razón que combinan acciones analgésicas, sedantes y hemodinámicas. Recientes estudios, que utilizaron BIS como indicador de nivel de hipnosis, reportan reducciones de un 20% sobre el consumo de propofol y de un 40% sobre el de isoflurano con el empleo de la clonidina87-89.
Un estudio de Peden y cols. con dexmedetomidina en distintas dosificaciones, que utilizó comandos verbales y respuestas motoras al estímulo quirúrgico como indicadores de plano anestésico, si bien no es concluyente en cuanto al sinergismo de ésta con la combinación alfentanilo/propofol, muestra una reducción en el consumo de ambos para mantener un adecuado plano anestésico. La conclusión de este estudio es que las dosis requeridas de dexmedetomidina para reducir requerimientos de otros agentes (incluyendo a los halogenados) son elevadas, teniendo las mismas efectos secundarios severos como bradicardia intensa o paro sinusal90.
Al utilizar anestesia intravenosa total (TIVA), es de vital importancia tener una vía venosa con segura permeabilidad —lo ideal es tener una “línea dedicada” para ese solo fin— y bombas de infusión que garanticen el suministro requerido de los agentes en uso.
Aquí también se debe tener en cuenta el fenómeno de la variabilidad farmacocinética individual, por lo que es recomendable el uso de dosis adecuadas y tablas o nomogramas que permitan la adecuación de los pesos corporales a las mismas, para evitar errores por exceso o por defecto; además del conocimiento de la farmacocinética y dinámica de los agentes utilizados. Por otra parte, en TIVA no se ha hallado todavía una manera práctica de medir la concentración en plasma, teniendo en cuenta, además, que el lugar de efecto de los anestésicos ocurre en la biofase, en el sistema nervioso central, y no en el plasma.
Enfatizar, una vez más, la necesidad de evitar comentarios despectivos por parte del equipo quirúrgico respecto al paciente o por hallazgos intraoperatorios. Procesos cog-nitivos de información escuchada durante niveles anes-tésicos aparentemente adecuados pueden ocurrir y resultar en daño psicológico.
Considerar ofrecer al paciente un consentimiento informado, si la condición médica lo permite, acerca de la posibilidad de que pueda llegar a tener algún recuerdo del transcurrir intraoperatorio, evitando amedrentarlo. Este hecho debe destacarse en condiciones en las que, por anticipado, sabemos que se administrarán niveles superficiales de anestesia, como por ejemplo cesáreas, trauma, o si por la condición fisiopatológica del paciente anticipamos la ocurrencia de inestabilidad hemodinámica24.
Detectar en la evaluación preoperatoria experiencias anestésicas pasadas, sobre todo si se detectan efectos posteriores desfavorables, y recordar que un antecedente de esa índole puede indicar una sensibilidad disminuida a los agentes anestésicos.
Instituir la visita postanestésica como medio para detectar y, eventualmente, tratar pacientes que puedan haber sufrido estado de inconciencia parcial91.
Lo cierto es que los pacientes pueden tener un estado de inconciencia parcial por muchas razones. Una de importancia es la insuficiente cantidad de anestésico administrado, lo que indica una falla en la técnica utilizada. En un estudio efectuado por Seppo y col. en Finlandia se observó que los pacientes que tuvieron despertares intraoperatorios habían recibido dosis menores de anestésicos que los demás pacientes. Así, la premedicación y administración continua, en dosis suficientes, son maneras de reducir la incidencia del fenómeno. A este concluyente hallazgo se oponen las presiones de tipo administrativo para reducir los tiempos entre cada cirugía con técnicas ”fast-track”, en las que se prioriza la velocidad de recuperación, a veces, a costa del nivel de anestesia suministrado92.
Otras causas son la tolerancia a los anestésicos, como la que pueden desarrollar los adictos a drogas, uso crónico de opioides o anfetaminas y el tabaquismo, ya que aumentan los requerimientos de las dosis necesarias para provocar inconciencia93.
Así como existe la denominada variabilidad interindividual, también deben considerarse las variaciones etarias y de contextura física. Si bien debiera tomarse en consideración el peso magro del paciente —es decir, sin tener en cuenta la masa grasa corporal— para el ajuste de dosis, puede ser difícil discernir el peso a tener en cuenta, aunque existan fórmulas y nomogramas para ese fin. En el reporte de la Dra. Domino18 aparecen fallas en el cálculo de incremento de dosis en obesos mórbidos en un 13% de los casos con estado de inconciencia parcial.
Otros motivos expuestos son la necesidad de discontinuar el suministro de anestésicos ante una repentina hipotensión, que no responde al tratamiento, o durante la cesárea, en la cual se reducen los requerimientos anestésicos para minimizar la depresión fetal17.
Respecto a los cambios en el comportamiento postope-ratorio de pacientes que sufrieron EIP, J. Andrade, en un editorial del British Journal94 se pregunta si las reacciones emocionales anómalas sólo ocurren después de cirugía con anestesia en planos superficiales. Deberíamos, entonces, evaluar los beneficios de aumentar las dosis de anestésicos y sus efectos potenciales sobre la recuperación.
Si a pesar de eso siguen ocurriendo tales reacciones, debieran implementarse soluciones alternativas, tales como aumentar la analgesia e hipnosis. La amnesia únicamente puede no ser un objetivo suficientemente bueno o deseable; pero hasta que el tema se termine de investigar y definir, es el más fácil de alcanzar94.
Algunos han refutado este objetivo relativamente fácil de alcanzar; pues se sugiere que, si hay recuerdo transope-ratorio, pudiera ser mejor para el paciente relatar la experiencia y no tener el episodio desagradable en un nivel subconciente95.
Conclusión
A pesar de contar con mejores fármacos y conocer más acabadamente sus mecanismos de acción en el SNC, todavía existe la posibilidad de tener pacientes que sufran EIP. Todo anestesiólogo debe ser conciente de la importancia de reconocer que, pese a su baja incidencia, es un hecho que puede ocurrir y, en consecuencia, debe ser prevenido y tratado.
El uso de tecnología adecuada haga probablemente descender su ocurrencia, pero hasta que dichas innovaciones sean accesibles en la práctica diaria, debemos aprovechar todos los conocimientos y recursos que la farmacología provee para que, junto a un criterio clínico preciso, se evite el síndrome descripto, así como secuelas emocionales para el paciente y económicas para la sociedad.
Bibliografía
- Liu WHD, Thorp AS, Graham SG, Aitkenhead AR. Incidence of awareness with recall during general anaesthesia. Anaesthesia 1991; 46: 435-437.
- Myles PS et al. Patient satisfaction after anaesthesia and surgery; results of a prospective survey of 10.811 patients. Br. J. Anaesth. 2000; 84: 6-10.
- Rampil IJ. Correspondence. Anesthesiology 1999; 90: 1798.
- Ghoneim MM. Awareness during anesthesia. Anesthesiology 2000; 92: 597-602.
- Griffith H, Jhonson G. Use of curare in general anesthesia. Anesthesiology 1942; 3: 418-420.
- Eich E, Reeves J, Katz R. Anesthesia, amnesia and the memory/awareness distinction. Anesth. Analg.1985; 64: 11436.
- Jones JG. Depth of Anaesthesia. Clinical Anesthesiology. London, Balliere Tindall (1989).
- Biescas Prat, Moix Queraltó, Casanovas Cator P. Análisis de la memoria implícita durante la hipnosis farmacológica con propofol. Rev. Esp. Anest. Reanim. (2000) 47: 458-463-8.
- Scott D. Awareness during general anesthesia. Canad. Anaesth. Soc. 1972; 19, 2:173-183.
- Eger E, Koblin D, Harris R et al. Hipotesis: Inhaled anesthetics produce immobility and amnesia by different mechanism at different sites. Anesth. Analg. 1997; 84, 915-918.
- Jones JG, Leary T. Awareness and total intravenous anesthesia. In: Total Intravenous Anesthesia Nicholas Padfield editor, Butterworth-Heinemann.Great Britain (2000), pág. 87-115.
- Artusio JF. Ester analgesia during major surgery. J. Am. Medical Association 1955; 157: 33-36.
- Levinson BW. Statess of awareness during general anaesthesia. Preliminary communication. Brit. J. Anaesth. 1965; 37: 544-546.
- Baileyand AR, Jones JG. Patients memories of events during general anaesthesia. Anaesthesia 1997; 52: 460-476.
- Vernon J, Sebel P. Memory and Awareness in Anesthesia. Seminars in Anesthesia 1993; XII, 3: 123-131.
- Ghoneim MM. Awareness during anaesthesia: a prospective case study. Lancet 2000; 355: 707-711.
- Operating room risk management. Awareness during Anesthesia. Ecri Technology Assesment Guide for Emerging technologies 2000, ECRI publisher. Chapter 14; pág. 1-6.
- Domino K, Posner K, Caplan R, Cheney F. Awareness during Anesthesia. A Closed Claims Analysis. Anesthesiology 1999; 90; 1053-61.
- Willwerth J, Planck N. Whats up, Doc?; its every surgery patients nightmare: youre awake enough to feel the knife but not enough to scream.Time (International edition) April 27,1998: 45.
- Hargrove R. Awareness under anesthesia. J. Medical Defense Union.1987; 3: 9-11.
- Cooper J, Newbower RS, Kitz RJ. An analysis of major errors and equipment failures in anesthesia management. Considerations for prevention and detection. Anesthesiology 1984; 60: 34-42.
- Chopra V, Bovill JG, Spierdijk J. Accidents, near accidents and complications during anaesthesia. A retrospective analysis of a 10 year period in a teaching hospital. Anaesthesia 1990; 45: 3-6.
- Aitkenhead A. Awareness during anaesthesia: what should the patient be told? Anaesthesia, 1990; 45: 351-352.
- McLeskey CH. Awareness during anesthesia. Refresher Course Outline. Can. J. Anesth. 1999; 46, 5: R80-R83.
- White P. Clinical Uses of Intravenous Anesthetic and Analgesic Infusions. Anesth. Analg. 1989; 68: 161-71.
- McCarthy GJ. Awareness during total intravenous anesthesia and how to avoid it. Annual Scientific Meeting, Belfast, november 2000.
- Brice D, Hetherington R, Utting J. A simple study of awareness and dreaming during anaesthesia. Brit. J. Anaesth. 1970; 42: 535-541.
- Seppo O, Ranta V, Riita L, Saario et al. Awareness with recall during anesthesia: incidence and risk factors. Anesth. Analg. 1998; 86: 1084-9.
- 29. Nordstrom O, Engstrom AM, Persson S, Rsandin. Incidence of awareness in total i.v. anaesthesia based on propofol, alfentanil and romuscular blockade. Acta Anaesth. Scand. 1997; 41: 978-84.
- 30. Utting JE. Pitfalls in anaesthetic practice. Br. J. Anaesth. 1987; 59, 877-890.
- Luble G, Kerssens MA, Phaf H, Sebel P. Dependence of explicit memory on hypnotic state in trauma patients. Anesthesiology 1999; 90: 670-
- Bonke B, Schmitz P, Verhage F et al. Clinical study of so-called unconcius perception during general anesthesia. Br. J. Anaesth. 1986; 58: -964.
- Coetzee J, Glen J, Wium C, Boshoff L. Pharmacokinetic model selection for target controlled infusions of propofol. Assessment of three ameter sets. Anesthesiology 1995; 82: 1328-45.
- Struys M, Mortier E, Versichelen L. Strategies to prevent awareness. On the study and practice of intravenous anesthesia. Edited by Vuyk Engbers F and Groen-Mulder S. Kluwer Academic Publishers. The Netherlands. pp.113-127.
- Eger E, Sadman I, Brandstater B. Minimun alveolar anesthetic concentration: A standard of anesthetic potency. Anesthesiology 1965; 26: -763.
- Prys-Robert C. Anesthesia: a Practical or Impractical Construct? Br. J. Anaesth. 1987; 59: 1341-1345.
- Zbinden A, Petersen-Felix S, Thomson D. Anesthetic depth defined using multiple noxius stimuli during isoflurane/oxygen anesthesia. odynamic responses. Anesthesiology 1994; 80: 261-267.
- Iselin-Chaves I, Flaishon R, Sebel P et al. The effect of the interaction of propofol and alfentanil on recall, loss of consciouness, and the bispectral index. Anesth. Analg. 1998; 87: 949-55.
- Kissin I. General Anesthetic Action: An Obsolete Notion? Anesth. Analg. 1993; 76: 215-218.
- Kissin I. A concept for assessing interactions of general anesthetics. Anesth. Analg.1997; 85: 204-10.
- Tanelian D, Kosek P, Mody I. The role of the GABA a receptor/chloride channel complex in anesthesia. Anesthesiology 1993; 78: 757-76.
- Glass P. Why and how we will monitor the state of anesthesia in 2010? Acta Anaesth. Belg. 1999; 50: 35-44.
- Glass P. An insight into general anesthesia-its mechanism and dosing strategies. Anesthesiology 1988;1, 88: 5-6.
- Katoh T, Ikeda K. The effects of fentanyl on sevoflurane requeriments for loss of conciusness and skin incision. Anesthesiology 1998; 88: 18-24.
- Kazama T, Ikeda K, Morita K. Reduction by fentanyl of the Cp50 values of propofol and hemodynamic responses to various noxious stimuli. Anesthesiology 1997; 87: 213-217.
- Drummond JC. Monitoring depth of anesthesia. Anesthesiology 2000; 93: 876-82.
- Watcha MF, White PF. Failure of lower esophageal contractility to predict patient movement in children anesthetized with halotano and nitrous oxide. Anesthesiology 1989; 71: 664-8.
- Pomfrett CJ. Heart rate variability, BIS and “depth of anaesthesia”. Br. J. Anaesth. 1999; 82, 5: 659-662.
- Pomfrett C, Barrie J, Healy T. Respiratory sinus arrhythmia reflects surgical stimulation during light enflurane anesthesia. Anesth. Analg. 1994; 78: 344.
- Greenwald S, Glass P, Payne F, Roscow C, Sebel P, Devlin P. Changes in heart rate variability predict responses during anesthesia. Anesthesiology 1998; 89: A898.
- Alkire M. Quantitative EEG correlations with brain glucose metabolic rate during anesthesia in volunteers. Anesthesiology 1998; 89: 323-33.
- 52. Sebel PS, Bowles SM, Saini V, Chamoun N. EEG bispectrum predicts movement during thiopental/isoflorane anesthesia. J. Clin. Monit. 5; 11: 83-91.
- Bowdle AT. Bispectral Index Monitoring. Annual meeting debate. Uses. The Society for Ambulatory Anesthesia. Samba 1999. www.sambahq.org/professional-info/education/abstracts/WS3/Bowdle
- Traast HS, Kallman CJ. Electroencefalografic characteristics of emergence from propofol/sufentanil total intravenous anesthesia. Anesth. Analg. 1995; 81: 366-71.
- Glass PS, Bloom M, Kearse L, Rosow C, Sebel P, Manberg P. Bispectral analysis measures sedation memory effects of propofol, midazolan, isoflurane and alfentanil in healthy volunteers. Anesthesiology 1997; 86: 836-47.
- Gan TJ, Glass PS, Windsor A, Payne F, Rosow C, Sebel P et al. Bispectral index monitoring anesthesia. BIS Utility Study Group. Anesthesiology 1997; 87: 808-15.
- Smith I, White P, Hahn CE, Adams AP. Total Intravenous Anesthesia. Principles and practice series1998; 98-127.
- Barr G, Jakobson, Owall A, Anderson RE. Nitrous Oxide does not alter bispectral index: study with nitrous oxide as sole agent and as adjunt to iv. Anaesthesia. Br. J. Anaesth. 1999; 82(6): 827-30.
- Silva et al. EEG biespectral index monitoring improves drug management during anesthesia. Anesthesiology 1997; 873a, 499.
- Loveman E, Van Hooff, Smith DC. The auditory evoked response as an awareness monitor during anaesthesia. Brit. J. of Anaesth. 2001; 86, 4: 513-8.
- Doj M, Gajraj RJ, Mantzaridis H, Kenny GNC. Relationship between calculated blood concentration of propofol and EEG variables. Anaesthesia 1997; 78: 180-4.
- Tufano R, De Robertis E, Servillo G. Depth Control Of Anaesthesia: Introduction to the topic. Minerva Anestesiol. 2001; 67, 5: 32-33.
- Thornton C. Evoked Potentials for monitoring depth of anestesia. Minerva Anestesiol. 2001; 67, 5: 35.
- Schraag S, Bothner U, Gajraj R, Kenny G, Georgieff M. The performance of EEG Biespectral index and auditory evoked potential index to predict loss of consciousness during propofol infusion. Anesth. Analg. 1999; 89: 1311-5.
- Doj M, Gajraj RJ, Mantzaridis H et al. Prevention of movement at laryngeal mask airway insertion: comparisos of AEP index, BIS, SEF and median frecuency. Brit. J. Anaesth. 1999; 82: 203-207.
- Daunderer M, Schweender D. Depth of anesthesia, awareness and EEG. Anaesthesist 2001; 50, 4: 231-241.
- Mantzaridis H, Kenny GN. Auditory evoked potential index: a quantitative measure of changes in auditory evoked potentials during general anaesthesia. Anaesthesia 1997; 52, 11: 1030-6.
- Davies FW, Mantzaridis H, Kenny GN et al. Middle latency auditory evoked potentials during repeated transitions from conciousness to unconciousness. Anesthesia 1996; 51: 107-113.
- Litvan H, Jensen E, Maestre M, Galán J, Campos J et al. Comparación de la efectividad de un índice de potenciales evocados auditivos y un índice biespectral con los signos clínicos en la determinación de la profundidad hipnótica durante anestesia con propofol o sevoflurano. Rev. Esp. Anest.y Reanim. 2000; 47, 10: 447-57.
- Bojanic S, SimpsonT, Bolger C. Ocular microtemor: a tool for measuring depth of anaesthesia? Brit. J. of Anaesth. 2001; 86(4): 519-22.
- Katz S. The media and the BIS monitor. Anesthesiology 1999; 90 (6): 1796-8.
- Rampil I. The media and the BIS monitor. Anesthesiology 1999; 90 (6):1798.
- Todd M. The media and the BIS monitor. Anesthesiology 1999; 90 (6): 1797.
- Todd M. The position of Aspect. Anesthesiology 2000; 92 (3): 897.
- Caba F, Echevarría M, Morales R, Guerrero JA, Rodríguez R. Sinergismo de midazolan y propofol en la inducción de la anestesia. Rev. Anest. Reanim.1993; 40: 69-71.
- Veselis RA, Reinsel RA, Feschenko VA, Wronski M. The comparative amnesic effects of midazolan, propofol, thiopental and fentanyl at equisedative concentrations. Anesthesiology 1997; 87: 749-64.
- Aldrete J, Wright A. Concerning the acceptability of awareness during surgery. Anesthesiology 1985; 63: 460-461.
- Hugh C. Does opioids anesthesia exist? Anesthesiology 1990; 73:1-4.
- Paladino M. Elaboración de estrategias anestésicas frente a un paciente: criterios para la elección de drogas. Rev. Arg. Anest. 2000; 58, 4: 257-268.
- Ghoneim M, Block R. Learning and consciousness during general anesthesia. Anesthesiology 1992; 76: 279-305.
- Russell I. Conscius awareness during general anesthesia: relevance of autonomic signs and isolates arm movements as guide to depth of anesthesia. Bailleres Clin. Anaesthes.1989; 3: 511-32.
- Dwyer R, Bennett H, Eger E et al. Isoflorane anestesia prevents unconciuos learning. Anesth. Analg. 1992; 77: 107-12.
- Eger E, Lampe G, Wauk L, Whitendale P, Cahalan M, Donegan J. Clinical pharmacology of nitrous oxide: an argument for its continued use. Anesth. Analg. 1990; 71: 575-585.
- Brahams D. Anesthesia and the law. Awareness and pain during anesthesia. Anesthesia 1989; 44: 352.
- Bourne JG. Nitrous Oxide in dentistry. Lloyd –Luke, London, 1960, chap. 7, pág. 5.
- Wilson S,Vaughan R, Stephen C. Awareness, dreams and hallucinations associated with general anesthesia. Anesth. Analg. Current Researches 1975; 54, 5.
- Ferh S, Zalunardo M, Seifert B, Rentsch K, Rohling R, Pasch T, Spahn D. Clonidine decreases propofol requeriments during anaesthesia: effect spectral index. Brit. J. Anaesth 2001; 86 (5): 627-32.
- Gabriel A, Faryniak B, Sojka G, Czech T, Freye E, Spiss C. Clonidine: and adjunt in isoflorane NO2 /O2 relaxant anaesthesia. Effects on EEG power spectra, somatosensory and auditory evoked potentials. Anaesthesia 1995; 50: 290-6.
- Ghignone M, Calvillo O, Quintin L. Anestesia and hipertensión: the effect of clonidine on perioperative hemodynamics and isoflorane requeriments. Anesthesiology 1987; 67: 3-10.
- Peden C, Cloote A, Stratford N, Prys-Roberts C. The effect of intravenous dexmedetomidine premedication on the dose requeriment of propofol to induce loss of conciousness in patients receiving alfentanil. Anaesthesia 2001; 56: 408-413.
- Moerman N, Bonke B, Oosting J. Awareness and recall during general anesthesia. Facts and feelings. Anesthesiology 1993; 79, 3.
- Seppo O et al. Awareness with recall during general anesthesia: incidence and risk factors. Anesth. Analg. 1998; 86: 1084-9.
- Sia R. Consciousness during general anesthesia. Anesth. Analg. Current Researches 1969; 48, 3: 363-366.
- Andrade J, Jones JG. Is amnesia for intraoperative events good enough? Brit. J. of Anaesth. 1998; 80, 5: 575-576.
- Blacher RS. Awareness during surgery. Anesthesiology 1984; 61:1-2.