Héctor J. Lacassie: Instructor en Anestesiología. Pontificia Universidad Católica de Chile.
Dirección Postal: Marcoleta 367, piso 3, Santiago Chile.
e-mail: hlacassi@rdc.cl
Introducción
La cesárea es una de las cirugías más frecuentes en el mundo, y seguramente la cirugía obstétrica más frecuente, con una incidencia que varía entre países, centros hospitalarios e incluso entre grupos obstétricos1 entre el 23% y más del 50% de los embarazos2.
El tipo de anestesia que se emplea depende de múltiples factores, entre otros: disponibilidad de anestesiólogo, urgencia del procedimiento, estado preoperatorio materno, indicación de la cesárea, preferencia personal, etc.
Actualmente, el tipo de anestesia más usado para este tipo de procedimientos es la anestesia regional neuroaxial (epidural y/o subaracnoidea), que ofrece como ventajas el mantener a la madre despierta, lo que le permite un contacto precoz con el recién nacido; minimizar el riesgo potencial de aspiración del contenido gástrico; evitar la depresión neonatal por drogas de la anestesia general2 y asociarse a un riesgo 16 veces menor de mortalidad materna por causas anestésicas, si se lo compara con el de la anestesia general 3.
Anestesia subaracnoidea
En nuestro centro y en muchos otros4, la anestesia raquídea, o subaracnoidea, es una de las más usadas para la operación cesárea. La simplicidad de su técnica, la reproducibilidad de sus efectos, su escasa latencia, la profundidad del bloqueo motor y la baja masa de droga utilizada la sitúan como una técnica regional muy recomendable para este tipo de procedimientos.
Técnica
Al igual que en cualquier procedimiento quirúrgico, y siguiendo las recomendaciones internacionales para una anestesia regional5, se debe monitorizar a la paciente con electrocardiografía continua, oximetría de pulso y medición de presión arterial no invasiva.
Previamente a la administración de la anestesia se ha recomendado.prehidratar. a la paciente con una solución multielectrolítica en dosis de 10-20 ml x kg-1, para evitar un descenso en la presión arterial luego del bloqueo simpático propio de la anestesia regional neuroaxial. Sin embargo, éste es un punto controversial, ya que existen evidencias en contra del rol protector de la prehidratación contra la hipotensión al efectuar la comparación con pacientes a las que no se las prehidrató6. Diferente es la situación de la prehidratación con coloides, donde se han documentado cambios hemodinámicos que se correlacionan con una menor incidencia de hipotensión luego de la anestesia subaracnoidea7. La modificación hemodinámica más importante parece ser un aumento del débito cardíaco con el coloide administrado (HAES 6%), protegiendo a la paciente contra la hipotensión en forma dosis dependiente (tabla I).
Tabla I
Respuesta hemodinámica frente a la precarga con volumen, expresado como porcentaje de aumento o disminución con respecto a la basal8 |
| | SRL 1,5 lt | HAES 6% 0,5 lt | HAES 6% 1,0 lt |
| n | 12 | 12 | 12 |
| DC (%) | 11 | 15 | 43* |
| Ż PA (%) | 75 | 58 | 17* |
| SRL: Solución ringer lactato; HAES 6%: Hidroxi etil almidón al 6%. DC: Débito cardíaco; PA: Presión arterial. *p<0,05 |
La posición de la paciente para realizar la punción subaracnoidea (decúbito lateral o posición sentada) dependerá de varios factores, entre los que se encuentran: baricidad de drogas, preferencia del anestesiólogo, contextura física materna, etc. Con respecto a los materiales, la aguja más utilizada es la de punta cónica (Whitacre, Sprotte o Gertie Marx®) y de calibre pequeño (25-27G); ambos factores son los más importantes en la prevención de la cefalea post punción dural9. Con dicha técnica, tenemos en nuestro centro una incidencia de ésta menor que el 1%, muy similar a lo reportado en la literatura para este tipo de materiales en la población obstétrica10. Existen agujas de menor calibre aun, con las que se logra una menor incidencia de cefalea post punción dural; sin embargo, se debe optar entre esto y una mayor dificultad de inserción de la aguja y de fracasos de la técnica. Probablemente, la aguja con el mejor perfil riesgo-beneficio sea la de calibre 27G con punta cónica no cortante (punta de lápiz).
Con respecto a las drogas, la más utilizada en nuestro centro es la bupivacaína 0,75% hiperbárica, asociada a fentanilo. Las dosis utilizadas son de 7,5-9 mg del anestésico local y 20 mg del opiáceo, con lo que se logra un nivel anestésico quirúrgico T2 [C7 -T5 ], con bloqueo motor completo (Bromage 1)11, que se recupera aproximadamente a los 90 minutos. La duración anestésica, definida como la regresión de 4 metámeras anestésicas, es de al menos 60 minutos12. De acuerdo con la literatura, lo más importante para un bloqueo subaracnoideo, en términos de calidad analgésica, es la masa de droga y no la baricidad de ésta, o el volumen en el cual es inyectada12,13. Existen otros esquemas de drogas con resultados variables (tabla II).
Tabla II
Dosis anestésicas subaracnoideas sugeridas para operación cesáre |
| Anestésico local | Opiáceo |
| Lidocaína 5% | Fentanilo |
| 50-80 mg | 10-25 mg |
| Bupivacaína 0.5% | Sufentanilo |
| 7-9 mg | 5-10 mg |
| El anestésico local puede combinarse indistintamente con uno de los opiáceos sugeridos. |
El uso de lidocaína hiperbárica por vía subaracnoidea para la operación cesárea tiene algunos inconvenientes, tales como su corta duración y el riesgo de producir un síndrome radicular transitorio. Esto es ampliamente descrito en diferentes tipos de cirugía, pero mucho más frecuentemente en aquellos casos en los que se usa lidocaína hiperbárica al 5% y en pacientes sometidos a cirugías en las que existe algún grado de sobreestiramiento de las raíces nerviosas, como, por ejemplo, la posición de litotomía14. A pesar de estos informes, la lidocaína hiperbárica sigue siendo la droga de elección para la cesárea de urgencia en numerosos centros, debido a su corta latencia en el inicio de acción.
Una vez administrada la anestesia, se posiciona a la paciente en decúbito dorsal con desplazamiento uterino hacia la izquierda.15ş a 30ş., para evitar el síndrome de hipotensión supino. Además se recomienda administrar oxígeno suplementario por una mascarilla facial, para aumentar la pO2 tanto materna como fetal15 y para tener una reserva de oxígeno en caso de urgencia materna y/o fetal.
Todas las maniobras antes descritas pueden ser resumidas en un simple acrónimo (en inglés), útil para no olvidar cada uno de los puntos (tabla III).
Tabla III
Acrónimo recordatorio |
| A |
Attention |
| E | Ephedrine |
| I | Inclination |
| O |
Oxygen |
| U |
Upper sensitive segment |
| Attention: Atención y vigilancia de la paciente, en especial de la hemodinamia. Ephedrine: Efedrina profiláctica 4-8 mg iv. Inclination: Inclinación de la paciente 15º-30º a la izquierda. Oxygen: Oxígeno por mascarilla facial (FiO2 : 3050%). Upper sensitive segment: Nivel sensitivo alcanzado que permita iniciar la cirugía (más a cefálico que T5). |
Uno de los principales problemas de la técnica es la alta frecuencia de hipotensión arterial (25-85%), a pesar del uso de medidas profilácticas tales como desplazamiento uterino y prehidratación. Esta hipotensión puede ser asintomática, y evidenciarse sólo en el monitor de presión arterial, o bien presentarse con una amplia gama de síntomas tales como náuseas, vómitos, dificultad respiratoria, mareos y otros. Algunos autores recomiendan el uso de efedrina profiláctica 30-50 mg intramuscular, 15 minutos antes de la anestesia, o 5-10 mg endovenosos, inmediatamente después de la administración del anestésico2, que es la forma más usada en nuestro centro. Con esta medida se disminuye la incidencia de hipotensión sin afectar el flujo úteroplacentario16 ni al neonato, a pesar de que el paso placentario de efedrina es del 70%17.
Complicaciones
La técnica anestésica subaracnoidea ha estado siempreíntimamente ligada al diagnóstico de cefalea post punción dural. Existen factores dependientes de la técnica y otros de la población (tabla IV).
Tabla IV
Factores responsables en la incidencia de cefalea post punción meníngea |
| Técnica | Sin rol |
| • Calibre | • Reposo |
| • Nş de punciones | • C. Intratecal |
| • Diseño aguja | • Embarazo* |
| Paciente |
| • Edad |
| • Sexo (f > m) |
| • Embarazo* |
| * El embarazo constituye factor de riesgo por el sexo y edad de las pacientes. Sólo aumenta el riesgo si se punciona con una aguja de calibre 22G o mayor, y se asocia a pujos maternos intensos durante el parto18. |
Los materiales actualmente en uso han disminuido considerablemente su incidencia, reduciéndola a valores cercanos al 1% de cefalea luego de una punción con aguja cónica no cortante (Whitacre) calibre 25G en la población obstétrica, igualando la incidencia de cefalea post punción dural de la técnica epidural10, por lo que este factor no debería condicionar la elección de la técnica anestésica.
Otros efectos colaterales menos frecuentes, aunque no menos importantes, se pueden encontrar en un excelente artículo de revisión de Horlocker y Wedel19.
Anestesia epidural
La anestesia epidural para la cesárea es una técnica que se ha popularizado, en parte, por el gran aumento del uso de analgesia epidural para el trabajo de parto, con la posibilidad de aprovecharla para una eventual cesárea, y por otro lado, por la idea en la comunidad de que la anestesia regional tiene menor riesgo de morbimortalidad materna3 que la anestesia general.
Ventajas
Las ventajas de la anestesia epidural sobre la técnica subaracnoidea ya antes explicada son:
- a.- posibilidad de titulación de la dosis anestésica para alcanzar el nivel apropiado;
- b.- flexibilidad en la dosificación si se requiere más tiempo quirúrgico;
- c.- inicio de acción más lento, lo que permite la compensación materna frente a los cambios hemodinámicos producidos por el bloqueo simpático;
- d.menor bloqueo motor, que permitiría la deambulación precoz, disminuyendo el riesgo teórico de trombosis venosa profunda, y, finalmente,
- e.- la posibilidad de usar el catéter para analgesia en el postoperatorio2.
Desventajas
Las desventajas de la técnica incluyen: a.- una latencia prolongada en el inicio de acción, lo que la hace una técnica inapropiada para una cesárea de urgencia, y b.- el inconveniente de la necesidad de grandes masas de anestésicos locales, con el consiguiente riesgo de toxicidad sistémica, en el caso en que el catéter se encuentre intravascular, o bien de realizar una anestesia espinal total, si el catéter estuviera intratecal o, incluso, en el espacio subdural20.
Técnica
Las consideraciones preanestésicas de monitorización e hidratación son similares a las ya mencionadas para la anestesia subaracnoidea.
La punción epidural ha sido descrita extensamente; sin embargo, vale la pena detenerse en algunos aspectos de la técnica, como la ubicación del espacio epidural. Ésta se realiza por medio del procedimiento de pérdida de resistencia, que puede ser con líquido o aire. En un estudio prospectivo, con casi 4.000 pacientes, Aida y col.21 dividieron al azar a los pacientes que requerían una anestesia epidural. El primer grupo se realizó con la técnica de pérdida de resistencia al aire, mientras que el segundo fue con líquido (solución fisiológica). En los casos de punciones advertidas de duramadre-aracnoides, o bien de aquellos pacientes con un alto grado de sospecha de una punción meníngea accidental, caracterizados por una anestesia espinal alta o un bloqueo motor intenso, se realizó tomografía axial computada de cerebro, correlacionando los hallazgos con clínica de la cefalea (tabla V).
Tabla V
Comparación de la técnica de pérdida de resistencia al aire vs. solución salina para la técnica de punción epidural21 |
| | Aire | Líquido |
| N° de pacientes | 1.812 | 1.918 |
| Perforación [n (%)] | 48 (2.6%) | 51 (2.7%) |
| Cefalea [n (%)] | 32 (67%) | 5 (10%) |
| Pneumoencéfalo [%] | 94 | 0 |
Los hallazgos demostraron un aumento en la sintomatología de la cefalea secundariamente a la generación de neumoencéfalo, lo que sugiere que se debería preferir la técnica de pérdida de resistencia al líquido.
Una vez alcanzado el espacio epidural, se puede administrar la dosis anestésica por la aguja22 o bien introducir un catéter epidural y hacerlo a través de éste, siempre en forma fraccionada, para evitar una simpaticolisis brusca, con la consiguiente hipotensión, además de detectar un posible mal posicionamiento del catéter, ya sea que esté en el espacio intratecal o que se encuentre endovenoso. Esta simple medida permite redosificar a la paciente por un catéter funcionante y previamente probado.
La instalación de un catéter epidural es un procedimiento a ciegas, por lo que se debe recurrir al máximo de pruebas diagnósticas que orienten a una correcta ubicación deéste, con el mínimo riesgo y costo para la paciente. Debido a los cambios fisiológicos del embarazo, el plexo venoso peridural (plexo venoso de Battson) está ingurgitado, por lo que la incidencia de canalización venosa está aumentada entre 2 a 4 veces (5-15%) con respecto a la paciente no grávida (2-3%)23. La dosis de prueba, originalmente descrita por Moore y Batra24, incluía una dosis de anestésico local con epinefrina (lidocaína 45 mg y epinefrina 15 mg) en suficiente cantidad como para producir una anestesia subaracnoidea, si el catéter estaba en una posición intratecal, o bien lograr un aumento en la frecuencia cardiaca de al menos diez puntos sobre la basal, si se hallaba intravascular. Con esta técnica se pensó que el dilema de la ubicación del catéter estaba solucionado; sin embargo, el comportamiento hemodinámico de la paciente embarazada es singular y enmascara posibles respuestas frente a las drogas vasoactivas, lo que le quita sensibilidad y especificidad a esta prueba. Hasta el momento, la maniobra con mejor perfil costo-beneficio para detectar una mala posición de catéteres instalados para analgesia durante el trabajo de parto es lo reportado por Norris et al23. En un estudio prospectivo, realizado en más de un millar de pacientes en trabajo de parto, se utilizó la tríada:
1.- aspiración secuencial del catéter,
2.- uso de dosis fraccionadas y
3.- drogas diluidas, para
probar un catéter epidural multiorificial. Con esta técnica se obtuvo un muy bajo porcentaje de falsos negativos, lo que sugiere que la analgesia epidural para el trabajo de parto puede ser administrada sin el uso de la tradicional dosis de prueba23. Sin embargo, si bien esto no puede ser extrapolado a la anestesia epidural quirúrgica necesaria para una operación cesárea, nos acerca a la respuesta del problema. Así, las recomendaciones para probar el catéter deberían incluir esos hallazgos, entre otros (tabla VI)
| Tabla VI |
| Recomendaciones para aumentar la sensibilidad en la detección de un catéter epidural mal ubicado (intratecal o intra vascular) |
| 1) Aspiración secuencial |
| 2) Dosis fraccionada |
| 3) Dosis de drogas adecuadas |
| 4) Observación permanente |
| 5) Uso de epinefrina |
| 6) Catéter multiorificio |
Las drogas que frecuentemente utilizamos por vía epidural son mezclas de anestésicos locales, opiáceos y coadyuvantes como la epinefrina. La racionalidad del uso de opiáceos como fentanilo o sufentanilo radica en su capacidad de potenciar la analgesia en forma aditiva o sinérgica25, de disminuir la incidencia de náuseas y vómitos durante la manipulación uterina y de disminuir los requerimientos de sedación endovenosa suplementaria, sin efectos adversos maternos2 ni fetales26, además de proporcionar analgesia postoperatoria15.
El esquema de drogas más usado en nuestro centro se muestra en la tabla VII.
Tabla VII
Esquema anestésico epidural frecuentemente usado para cesárea |
| Droga |
Dosis |
| Bupivacaína |
40-60 mg |
| Lidocaína | 100-200 mg |
| Fentanilo o | 50-100 mg |
| Sufentanilo | 10-20 mg |
| Volumen total | 15-24 ml |
Con esta dosificación se obtiene un nivel anestésico suficiente (T4 -T5) como para realizar una cesárea sin exponer a la paciente a altas dosis de anestésicos, como ocurre con algunos esquemas sugeridos en la literatura, en los que se usa en forma habitual 75-125 mg de bupivacaína2 como droga única.
En algunas ocasiones es necesario utilizar algún tipo de sedación, ya sea para tratar la ansiedad materna o bien para suplementar bloqueos incompletos (20% de las anestesias epidurales22), en especial, el dolor visceral que aparece al manipular peritoneo, o frente a la tracción de estructuras intraabdominales, como ocurre en la cuestionable exteriorización uterina. Las técnicas de suplementación más usadas son la administración por mascarilla facial de óxido nitroso en oxígeno 50%, ketamina en bolos pequeños (0,10,25 mg x kg-1) o bien el uso de opiáceos sistémicos tales como fentanilo (0,5-1 mg x kg-1)15 o el opiáceo de elección en nuestro centro, el remifentanilo. Este último es un opiáceo m agonista con características farmacológicas muy interesantes, tales como:
- ultra corta duración, dada por su metabolización sobre la base de hidrólisis enzimática por esterasas inespecíficas que se encuentran en sangre y tejidos, que impide su acumulación en el tiempo, incluso luego de su administración en forma continua.corta vida media contextual (CSt1/2).;
- alta potencia, similar a la del fentanilo;
- breve inicio de acción, dado por su bajo tiempo para equilibrarse en el sitio de efecto (t1/2 keO)27.
A todo esto se agregan las evidencias presentadas por Kan et al28 al analizar los casos de 19 pacientes sometidas a operación cesárea bajo anestesia regional, en las que se usó remifentanilo para sedación por medio de una infusión endovenosa continua a 0,1 mg x kg-1 x min-1. En estas condiciones se evidenció que existe un paso transplacentario de la droga por encima del 85%, que es metabolizada en gran medida por el feto, por lo que al nacer, los niveles plasmáticos fetales de remifentanilo no se traducen en depresión neonatal27. Pero por otra parte, la dosis administrada se asoció a depresión respiratoria y sedación maternas, caracterizadas, en una escala de sedación, por un valor 2 a 3 de 5, lo que corresponde a paciente somnolienta y con los ojos cerrados, pero fácilmente despertable. Es así que pensamos que las dosis endovenosas de remifentanilo para sedación en cesárea deberían ser menores a las reportadas por Kan et al., es decir: 0,02 a 0,06 mg x kg-1 x min-1.
Efectos colaterales
Las complicaciones de la técnica epidural para la cesárea no difieren en gran medida de las de la técnica epidural en general (tabla VIII).
Anestesia combinada espinal-epidural
La anestesia combinada espinal-epidural para la cesárea fue descrita por Brownridge29 en 1981. Esta técnica reúne lo mejor de ambas técnicas, vale decir, la rapidez y la profundidad anestésica del componente espinal y la flexibilidad de la epidural al titular la dosis o bien prolongar la anestesia
Tabla VIII
Algunas de las complicaciones más graves de la técnica anestésica epidural |
| Punción meníngea accidental |
| Anestesia espinal total |
| Anestesia subdural |
| Toxicidad por anestésicos locales |
| Hematoma epidural |
| Lesiones neurológicas |
tanto como el procedimiento lo requiera30.
En los tiempos actuales, donde los principales determinantes de nuestro accionar son tanto la paciente como el costo y la eficiencia del método anestésico utilizado, esta técnica permite una optimización de los resultados, ya que al administrar una dosis anestésica intratecal se logran bloqueos confiables, con corta latencia, lo que permite el rápido inicio de la cirugía, sin producir alteraciones hemodinámicas importantes, que es el principal problema de la anestesia subaracnoidea cuando se la utiliza como técnica única. Al titular el nivel anestésico requerido a través del componente epidural, se logra una mejor analgesia, y con menos hipotensión que cuando se administraúnicamente una anestesia epidural31. Finalmente, el perfil de seguridad de la técnica es alto, ya que se usa una baja masa de droga, minimizando así los riesgos de toxicidad sistémica si se produjera accidentalmente una inyección intravascular.32
Técnica
Las consideraciones preanestésicas de monitorización e hidratación deben ser las mismas que las aplicadas para las técnicas epidural y subaracnoidea. Con respecto a la punción epidural, se deben seguir las mismas directrices que ya se han mencionado para cuando se la utiliza como técnicaúnica.
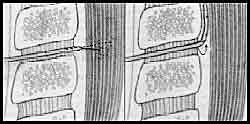
Al puncionar con la aguja espinal se recomienda previamente girar el bisel del trocar epidural hacia caudal y luego, cuando se va a introducir el catéter epidural, volver a girar el bisel 180ş hacia cefálico. Esta maniobra reduciría, al menos en teoría, la posibilidad de una cateterización subaracnoidea accidental a través de la perforación dejada por la aguja espinal, ya que al realizar esto con la técnica de aguja a través de aguja se produciría una leve deflexión de la aguja espinal hacia caudal y luego una deflexión del catéter hacia cefálico (figura 1).
[ Ampliar imagen ] |
| Figura 1: Dibujo esquemático de la rotación en 180º del bisel de la aguja epidural. En el panel izquierdo se ve la deflexión de la aguja espinal y, con una línea punteada, el eje mayor de la aguja epidural. En el panel derecho se observa la dirección adoptada por el catéter epidural. |
Sin embargo, al realizar la maniobra de giro, existe el riesgo de perforar con la punta de la aguja epidural la dura-aracnoides.32
Al usar el catéter epidural para suplementar el bloqueo subaracnoideo, se debe tener en mente que existe una perforación meníngea, que va a favorecer el paso de drogas del espacio epidural al subaracnoideo, proporcional al tamaño del orificio dejado en la dura-aracnoides33,34. Por eso se debe tener precaución en el uso de refuerzos anestésicos por vía del catéter epidural, los que deben ser menores que los que se utilizan en una anestesia epidural tradicional.
Las dosis anestésicas recomendadas para la operación cesárea son menores que las usadas tradicionalmente en la anestesia subaracnoidea. Actualmente, la droga más utilizada es la bupivacaína asociada a un opiaceo (fentanilo o sufentanilo). Ocasionalmente se puede agregar coadyuvantes como epinefrina, clonidina y/o neostigmina. Las dosis recomendadas pueden verse en la tabla IX.
Tabla IX
Dosis sugeridas para realizar una anestesia combinada epidural espinal en operación cesárea |
| Componente intratecal |
| Droga | Dosis |
| Bupivacaína | 3-6,6 mg |
| Fentanilo o | 10-25 mg o |
| Sufentanilo | 3,3-10 mg |
| Componente epidural |
| Droga | Dosis |
| Lidocaína 2% | 2 ml / segmento no bloqueado35 |
| Bupivacaína | 20-40 mg |
| Solución fisiológica* | 10 ml |
| * El uso de solución fisiológica para aumentar el nivel del bloqueo sensitivo debe realizarse dentro de los primeros 30 minutos de la administración de la dosis subaracnoidea36-37. |
Con el tiempo, la dosis intratecal de bupivacaína se ha ido reduciendo, hasta llegar a niveles realmente bajos, con mínima repercusión hemodinámica y con una muy baja incidencia de molestias intraoperatorias. La necesidad de suplementar la anestesia subaracnoidea con dosis epidural por el catéter varía del 10 al 100% de los casos, dependiendo de varios factores tales como dosis intratecal, técnica quirúrgica (exteriorización uterina), duración de la cirugía, etc.
Efectos colaterales
Como la técnica combinada es una mezcla de dos técnicas, los efectos colaterales deberían ser la suma de los problemas de cada una de ellas. Sin embargo, esto no ha podido ser demostrado para cada uno de los problemas, o incluso se ha planteado un valor protector contra algunos de ellos.
Los problemas potenciales de esta técnica son, entre otros:
- falla de la técnica al no identificar el espacio subaracnoideo;
- no reflujo de líquido céfalo-raquídeo por la aguja espinal, ya sea por mala posición de la aguja epidural, que desvía a la espinal, o por punciones tangenciales al saco dural;
- dificultaden el momento de instalar el catéter epidural luego de haber administrado la dosis de anestésico local intratecal, que lleva a riesgo de lateralización (paciente en decúbito lateral) de la anestesia subaracnoidea o a una anestesia muy baja (paciente sentada);
- canulación venosa con el catéter epidural;
- perforación meníngea con el catéter a través del orificio dejado por la aguja espinal (lo que se debe considerar extremadamente raro, ya que en un modelo en cadáveres, bajo visión por epiduroscopía, luego de la punción subaracnoidea con una aguja calibre 25G, no fue posible pasar un catéter epidural calibre 18G por la perforación38);
- presencia de un catéter no probado con anterioridad al momento en que se requiere su funcionamiento;
- arrastre de partículas metálicas de la aguja epidural al realizar la técnica.aguja a través de aguja. (needle through needle);
- infección meníngea; etc.
Con recto al riesgo de presentar cefalea post punción meníngea al puncionar intencionalmente la duramadrearacnoides con una aguja espinal, sumado al riesgo de punción meníngea accidental con la aguja epidural, la lógica dice que debería aumentar la incidencia de cefalea si se establece la comparación con cada una de las técnicas por separado. Sin embargo, se ha demostrado que no es así, e incluso la técnica combinada sería un factor protector39. Esto debe ser interpretado con precaución, ya que los centros que han evaluado este punto tienen amplia experiencia en la técnica combinada y han realizado estudios no ciegos, lo que les confiere un sesgo a los resultados.
Analgesia post-cesárea
La cirugía produce daño tisular, con las consecuentes liberación de sustancias algésicas (prostaglandinas, histamina, serotonina, bradikininas, sustancia P y otras) y generación de estímulos nocivos que son detectados por nociceptores y transmitidos por fibras A delta (d) y C hacia el neuroeje. El resto de la transmisión está determinada por influencias moduladoras complejas en el nivel de la médula espinal. Algunos impulsos pasan a los cuernos anteriores y antero-laterales de la médula espinal, provocando respuestas reflejas segmentarias. Otros son transmitidos a centros superiores a través de los haces espinotalámicos y espinoreticulares, generando respuestas suprasegmentarias y corticales. Las respuestas a los reflejos segmentarios asociados a cirugía incluyen aumento del tono muscular y espasmos, con el consecuente incremento del consumo de oxígeno muscular y de la producción de ácido láctico. La estimulación de neuronas simpáticas produce taquicardia, aumento del volumen sistólico eyectado y del trabajo cardíaco, acrecentando el consumo de oxígeno miocárdico. El tono de la musculatura lisa disminuye en el nivel del aparato gastrointestinal y genitourinario. La respuesta de reflejos suprasegmentarios resulta en un incremento más marcado del tono simpático, con el consiguiente aumento de la respuesta en los diferentes sistemas40.
El dolor experimentado en el postoperatorio de una cesárea es similar al de aquellas cirugías intraabdominales infraumbilicales, vale decir: agudo, de intensidad moderada, de mayor magnitud en las primeras 6 horas y referido a la piel entre las metámeras T9 a L1, con predominio del dolor de tipo incidental (con los movimientos). El dolor generado en los músculos y aponeurosis es somático, mientras que el originado en el útero y peritoneo es visceral40.
Técnicas analgésicas
El manejo del dolor puede realizarse de múltiples formas, dependiendo de la experiencia y de los recursos disponibles en cada centro. Las alternativas más usadas son la analgesia regional y la sistémica.
Analgesia regional:
Es la técnica ideal, en la que se usan anestésicos locales y/ u opiáceos neuroaxiales. Los primeros interrumpen la transmisión del dolor somático y visceral transmitido por los haces espinotalámicos, suprimiendo por completo la respuesta neuroendocrina41. Los opiáceos como droga única son igualmente efectivos en este tipo de cirugía; sin embargo, dado su mecanismo de acción, no bloquean la respuesta neuroendocrina sino que sólo modulan las vías nociceptivas del SNC. Las técnicas regionales permiten que la paciente esté libre de dolor durante el postoperatorio usando drogas de muy bajo costo, como puede ser el caso de la morfina, y que deambule en forma precoz al no tener bloqueo motor. Esta capacidad de movilización precoz le confiere a la técnica un valor agregado, ya que la paciente embarazada o en el puerperio inmediato tiene un estado de hipercoagulabilidad.debido al aumento en los niveles de factores de coagulación., lo que sumado al reposo en cama del postoperatorio incrementa el riesgo de que presente trombosis venosa profunda de extremidades inferiores, con el eventual riesgo de tromboembolismo pulmonar42. El problema de esta técnica es la necesidad de control permanente de las pacientes, en particular de aquellas con morfina neuroaxial, ya que existe un riesgo clásicamente descrito de depresión respiratoria bifásica que puede aparecer a los 3090 minutos de administrada la morfina por vía epidural (no así para la administrada por vía espinal) y, luego, a las 6-12 horas de la administración de la morfina por vía tanto epidural como subaracnoidea42. Esta depresión respiratoria es leve y en la mayoría de los casos no requiere reversión con antagonistas de opiáceos; sin embargo, dado el riesgo que potencialmente existe, se sugiere el control horario de frecuencia respiratoria durante las primeras 12 a 14 horas y se aconseja no administrar sedantes tales como benzodiazepinas, ya que éstas aumentan el riesgo de depresión respiratoria.
Las dosis recomendadas de morfina epidural son 2 a 2.5 mg. Para el caso de la analgesia subaracnoidea con morfina, la dosis equipotente a la epidural es de 75 a 100 mg 43, lo que corresponde al 4% de la dosis epidural44. En este tipo de cirugía, un aumento en las dosis no incrementa la calidad analgésica pero sí los efectos colaterales43.
Al usar opiáceos epidurales/subaracnoideos es recomendable el uso de un antiinflamatorio no esteroidal como coadyuvante analgésico, ya que permite controlar el dolor de tipo incidental (incisión de la piel), que es resistente a los opiáceos.
Analgesia sistémica:
Por esta vía se pueden utilizar opiáceos (fentanilo, morfina, tramadol) y antiinflamatorios no esteroidales. La forma de administración puede ser por bolos, infusiones continuas o bien administración controlada por la paciente.patient controlled analgesia (PCA)., que le permite a ésta determinar la cantidad de analgésico que se administra, con lo que disminuyen los riesgos de depresión respiratoria u otros efectos colaterales y, además, se posibilita la reducción en el uso total de analgésicos.
El dolor de la incisión de la piel es bien controlado por antiinflamatorios no esteroidales y/o anestésicos locales, no así por los opiáceos. El dolor muscular y visceral responde muy bien a opiáceos. Los esquemas terapéuticos más frecuentemente usados son: 1.Tramadol 100 mg + ketorolaco 30 mg diluidos en suero glucosado 5% 500 ml, en infusión continua a 20 ml x h-1.
Con esta modalidad se mejora la calidad analgésica si se la compara con la administración en bolos45. 2.Bolos de 2 mg de morfina según necesidad + ketorolaco 30 mg o ketoprofeno 100 mg cada 8 horas. 3.PCA con morfina, con una programación [0-1-8], lo que significa: 0 = sin infusión continua; 1 = bolos de 1 mg por demanda del paciente; 8 = intervalo de seguridad de 8 minutos, es decir, la máquina entrega bolos cada 8 minutos o más. 4.Metamizol sódico 2 g cada 8 horas + morfina 2 mg según necesidad (este último esquema es el más utilizado en los hospitales estatales debido a su bajo costo). La analgesia debe ser usada en infusión continua, o por horario, y nunca debe ser indicada cuando la paciente esté experimentando dolor o este comience a reaparecer, ya que, dada la farmacocinética de los analgésicos, se debe esperar un lapso de tiempo hasta que la droga alcance niveles plasmáticos efectivos para el control del dolor.
El costo de los diferentes esquemas analgésicos debe ser evaluado con precaución, ya que no sólo se debe considerar el cargo por las drogas utilizadas sino también los costos paralelos, tales como: tratamientos adicionales cuando falla la técnica analgésica, tratamiento de efectos colaterales, costo por intervenciones del personal, materiales (PCA, bombas de infusión continua), etc. En la tabla X
Tabla X
Precios de los diferentes fármacos utilizados en la terapia de dolor postoperatorio en el Hospital Clínico de la Pontificia Universidad Católica de Chile |
| Droga | U$S |
| Morfina 10 mg | 0,5 |
| Meperidina 100 mg | 0,48 |
| Fentanilo 100 mg | 1,39 |
| Tramadol 100 mg | 0,21 |
| Ketorolaco 30 mg | 4,2 |
| Naloxona 0,4 mg | 1,39 |
| Bupivacaína 0,5% 20 ml | 2,17 |
| Droperidol 5 mg | 0,67 |
| Kit PCA Abbott | 14,1 |
| Los precios están expresados en dólares norteamericanos. |
se puede ver una comparación de costos en fármacos e insumos en nuestro centro.
Conclusiones
Se ha presentado una revisión de las técnicas de anestesia regional más usadas para la cesárea, junto con algunas de las alternativas actuales de analgesia postoperatoria para este tipo de cirugía.
Las técnicas descritas son el acopio de varios años de investigación y de desarrollo de cada una de ellas; sin embargo, no se debe olvidar que cuando aparecen varias técnicas para enfrentar un problema determinado, existen dos posibilidades que explican este hecho: el ingenio humano permite la creación de más de alguna solución para un problema dado o bien no hay aún ninguna respuesta óptima para resolver el problema, sino que hay varias mediocres. En el caso de la anestesia para la cesárea, las técnicas descritas son lo mejor que podemos hacer, pero se alejan considerablemente de la perfección. Esto no debe desalentarnos sino, por el contrario, estimularnos a investigar y mejorar lo que ya tenemos hasta lograr una técnica que beneficie aun más a nuestras pacientes, lo que debería ser nuestro fin último.
|
|
Bibliografía
-
Beilin Y, Friedman F, Bernstein H, Andres L, Bodian C. The obstetrician group, not epidural analgesia, influences the cesarean section rate for the nulliparous woman in labor. Anesth Analg. 1999; 88, S249.
- Reisner L, Lin D. Anesthesia for Cesarean Section, en: D. Chestnut, Obstetric Anesthesia. Principles and Practice. St Louis, MO, Mosby-Year Book Inc., 1994, pág. 459-86.
- Hawkins JL, Koonin LM, Palmer SK, Gibbs CP. Anesthesiarelated Deaths during Obstetric Delivery in the United States, 1979-1990. Anesthesiology, 1997; 86(2), 277-284.
- Holmstrom B, Rawal N, Arne S. The use of central regional anesthesia techniques in Sweden: results of a nation-wide survey. Acta Anesthesiologica Scandinavica, 1997; 40: 565572.
- American Society of Anesthesiologists Guidelines for Regional Anesthesia in Obstetrics. Appendix A, en: D. Chestnut, Obstetric Anesthesia. Principles and Practice. St Louis, MO, Mosby-Year Book Inc., 1994, pág. 1006-7.
- Rout C, Rocke D, Levin J, Gouws B, Reddy D. A reevaluation of the role of cristalloid preload in the prevention of hypotension associated with spinal anesthesia for elective cesarean section. Anesthesiology, 1993; 79, 262-269.
- Baraka A, Taha S, Ghabach M, Sibaii A, Nader A, MDibaii A. Intravascular administration of polymerized gelatin versus isotonic saline for prevention of spinal-induced hypotension. Anesth Analg. 1994; 78: 301-305.
- Hiroshi U, Yan-Ling H, Hironobu T, Takashi M, Ikuto Y. Effects of Crystalloid and Colloid Preload on Blood Volume in the Parturient Undergoing Spinal Anesthesia for Elective Cesarean Section. Anesthesiology, 1999; 91: 1571-1576.
- Halpern S, Preston R. Postdural puncture headache and spinal needle design. Metaanalyses. Anesthesiology, 1994, 81; 1376-1383.
- Lambert D, Hurley R, Hertwig L, Datta S. Role of needle gauge and tip configuration in the production of lumbar puncture headache. Reg Anesth. 1997, 22; 66-72.
- Bromage P. Epidural Analgesia, Philadelphia, WS Saunders, 1978: 144.
- Sarvela P, Halonen P, Kortilla K. Comparison of 9 mg of intrathecal plain and hyperbaric bupivacaine both with fentanyl for cesarean delivery. Anesth Analg. 1999, 89: 12571262.
- Malinovsky J, Renaud G, Le Corre P et al. Intrathecal Bupivacaine in Humans. Influence of volume and baricity of solutions. Anesthesiology, 1999; 91: 1260-1266.
- Lacassie HJ. Neurotoxicidad por lidocaína 5%: żDescrédito o realidad? Revista Chilena de Anestesia, 1998; 27, 2: 112-114.
- Shnider S, Levinson G. Anesthesia for Cesarean section, en: S. Shnider, G. Levinson, Anesthesia for Obstetrics, 3Ş ed. Baltimore, Maryland, Williams & Wilkins, 1993, pág. 211-245
- Ralston D, Shnider S, De Lorimier A. Effects of equipotent ephedrine, metaraminol, mephentermine and methoxamine on uterine blood flow in the pregnant ewe. Anesthesiology, 1974, 40; 354-370.
- Hughes S, Ward M, Levinson G. Placental transfer of ephedrine does not affect neonatal outcome. Anesthesiology, 1985, 63; 217-219.
- Ravindran RS, Viegas OJ, Tasch MD, Cline PJ, Deaton RL, Brown TR. Bearing down at the time of delivery and the incidence of spinal headache in parturients. Anesth Analg. 1981, 60: 524526.
- Horlocker T, Wedel D. Neurologic complications of spinal and epidural anestesia. Regional Anesthesia and Pain Medicine 2000, 25: 83-98.
- Glosten B. Local anaesthetic techniques, en: D.H. Chestnut (ed.), Obstetric Anesthesia. Principles and Practice. St. Louis, MO, Mosby Yearbook Inc., 1994: 370-371.
- Aida S, Taga K, Yamakura T et al. The Role of Intrathecal Air, Anesthesiology, 1998; 88: 76-81.
- Pernoll M, Mandell J. Cesarean section, en: John Bonica y John McDonald, Principles and Practice of Obstetric Analgesia and Anesthesia. 2Ş ed., Malvern PA, Williams & Wilkins, 1995, pág. 968-1009.
- Norris M, Fogel S, Dalman H et al. Labor Epidural Analgesia without an Intravascular.Test Dose., Anesthesiology, 1998; 88: 1495-1501.
- Moore DC, Batra MS. The components of an effective test dose prior to epidural block, Anesthesiology, 1981; 55: 693-696.
- Solomon R, Gebhart G. Synergistic antinociceptive interactions among drugs administered to the spinal cord, Anesth Analg. 1994; 78, 1164-72.
- Porter J, Bonello E, Reynolds F. Effect of Epidural Fentanyl on Neonatal Respiration, Anesthesiology, 1998; 89: 79-85.
- Glass P, Gan T, Howell S. A review of the pharmacokinetics and pharmacodynamics of remifentanil, en: Clinical pharmacology of remifentanil, Anesth Analg. 1999; 89, 4S, S7-S14.
- Kan R, Hughes S, Rosen M et al. Intravenous Remifentanil. Placental Transfer, Maternal and Neonatal Effects, Anesthesiology, 1998; 88: 1467-1474.
- Brownridge P. Epidural and subarachnoid analgesia for elective cesarean section. Anaesthesia, 1981; 36: 70.
- Fan S, Susetio L, Wang Y. Low dose of Intrathecal Hyperbaric Bupivacaine Combined with Epidural lidocaine for cesarean section. A balance block technique. Anesth Analg. 1994; 78, 474-477.
- Rawal N, Schollin J, Wesstrom G. Epidural versus combined spinal epidural block for cesarean section. Acta Anesthesiol Scand. 1988; 32: 61-66.
- Rawal N, Van Zundert A, Holmström B et al. Combined spinalepidural technique, Reg Anesth. 1997; 22: 406-423
- Swenson J, Wisniewski M, McJames S et al. The effect of prior dural puncture on cisternal cerebrospinal fluid morphine concentrations in sheep after administration of lumbar epidural morphine. Anesth Analg. 1996, 83: 523-525.
- Leighton B, Arkoosh V, Huffnagle S, Huffnagle H et al. The dermatomal spread of epidural bupivacaine with and without prior intrathecal sufentanil, Anesth Analg. 1996, 83: 526-529.
- Vercauteren M, Coppejans H, Hoffmann Vet al. Small-dose hyperbaric versus plain bupivacaine during spinal anesthesia for cesarean section, Anesth Analg. 1998; 86: 989-993.
- Takiguchi T, Okano T, Egaw H et al. The effect of epidural saline injection on analgesic level during combined spinal and epidural anestesia assessed clinically and myelographically, Anesth Analg. 1997; 85, 1097-1100.
- Stienstra R, Dahan A, Alhadi B et al. Mechanism of action of an epidural top-up in combined spinal epidural anesthesia, Anesth Analg. 1996, 83: 382-386.
- Holmstrom B, Rawal N, Axelsson K et al. Risk of catheter migration during combined spinal epidural block: percutaneous epiduroscopy study, Anesth Analg. 1995; 80: 747-753.
- Norris M, Grieco W, Borkowski M et al. Complications of labor analgesia: Epidural versus combined spinal epidural techniques. Anesth Analg. 1994; 79: 529-537.
- Lacassie H y Lacassie HJ. Anestesia en Obstetricia, en: A. Pérez y E. Donoso, Obstetricia, 3Ş ed., Santiago, Publicaciones técnicas Mediterráneo Ltda, 1999, pág. 400-416.
- Liu S, Carpenter R, Neal J. Epidural anesthesia and analgesia. Their role in postoperative outcome, Anesthesiology, 1995; 82: 1474.
- Sinatra R. Postoperative Analgesia: Epidural and Spinal Teschniques, en: D. Chestnut, Obstetric Anesthesia. Principles and Practice, St Louis, MO, Mosby-Year Book Inc., 994, pág. 513-547.
- Palmer C, Emerson S, Volgoropolous D. Dose-Response Relationship of Intrathecal Morphine for Postcesarean Analgesia. Anesthesiology, 1999, 90: 437-444.
- Cousins M, Mather L. Intrathecal and epidural administration of opioids, Anesthesiology, 1984, 61: 276.
- Lacassie HJ, Cortínez L, Muñoz H et al. Comparison of two tramadol administration schemes for post cesarean section analgesia. Regional Anesthesia and Pain Medicine, 1999; 24 (3) Supl., pág. 35.
|
