Dr. Juan Carlos Bianco (h): Médico residente de Anestesiología. Hospital Privado de Córdoba
Dr. Guillermo Galeotti: Anestesiólogo de planta del Hospital Privado de Córdoba
Introducción
La toracotomía es generadora de uno de los dolores postoperatorios más intensos y su manejo es un considerable desafío1. A pesar del desarrollo de variadas técnicas analgésicas, el dolor agudo y crónico post-toracotomías continúa siendo un problema.
La administración de morfina intratecal (IT) en humanos para analgesia postoperatoria registra la publicación de sus primeros trabajos mundiales en 1979 de Behar et al 2y Wang et al3. Mientras que la analgesia peridural goza de gran aceptación y es considerada el gold standard, los opiodes subaracnoideos se habían considerado de menor eficacia y seguridad a causa de la alta incidencia de reacciones adversas, tan graves como la depresión respiratoria. Sin embargo el posterior uso de mini dosis de morfina intratecal ( < 1 mg ) para el manejo del dolor postoperatorio agudo en una gran variedad de cirugías con índices bajos de depresión respiratoria, relacionó las complicaciones graves de la morfina intratecal con el uso de grandes dosis de ésta 4.
El propósito de este estudio fue determinar la eficacia, seguridad y reacciones adversas de la morfina IT en dosis única para el manejo del dolor agudo post toracotomías.
Materiales y Métodos
Con la aprobación del Comité de Ética se realizó un estudio prospectivo observacional en el Hospital Privado de Córdoba desde enero de 2001 a julio de 2003 con 39 pacientes que fueron sometidos a toracotomías, de los cuales se excluyeron dos, uno por error en la dosis de morfina IT y otro por falta de recolección de datos.
Los pacientes eran adultos (entre 18 y 77 años), hombres y mujeres, ASA I a III con toracotomías programadas en las que se evaluó la morfina IT en las primeras 36 hs posteriores a su aplicación.
Se excluyeron del estudio aquellos pacientes con:
- infección local o sistémica
- coagulopatías
- trastornos en la columna vertebral
- alergia a drogas
- apnea obstructiva del sueño
- falta de consentimiento del paciente
- edades mayores de 80 y menores de 15 años.
En el quirófano, una vez conseguida una vía endovenosa, se realizó premedicación con midazolam 1 – 3 mg EV. Con el paciente despierto se realizó la punción lumbar en posición sedente o en decúbito lateral en los espacios lumbares L2-L3, L3-L4 o L4-L5, bajo estrictas condiciones de asepsia con agujas Whitacre 27 G, hasta la visión de líquido cefalorraquídeo por la aguja, momento en el que se inyectó morfina sin conservantes intratecal en rango de dosis de 0,3 a 0,8 mg (media de 0,5 mg) a la que se asoció fentanilo en 15 pacientes (41,7%) en un volumen total medio de 2,5 ml (con un rango de 1,5 a 4 ml) el que se alcanzó agregándole solución fisiológica 0,9%.
La anestesia general se indujo con tiopental sódico 3 - 5 mg/kg con una administración previa de fentanilo de 1 – 3 ug/kg. Para facilitar la intubación se utilizó succinilcolina 1 mk/kg. La anestesia fue mantenida con anestésicos inhalatorios (isofluorane, sevofluorane o halotano), fentanilo y relajantes musculares (pancuronio, vecuronio).
El monitoreo incluyó:
- oximetría de pulso
- capnografía
- registro electrocardiográfico de 3 derivaciones
- monitoreo automático no invasivo de la presión arterial.
- Los indicadores para extubación fueron:
- recuperación de la conciencia
- respiraciones espontáneas y rítmicas y aceptable volumen repiratorio
- CO2 expirada < o = 45 mmHg
- estabilidad hemodinámica
- saturación > o = 95%.
Cuando los pacientes se quejaban de dolor en la Unidad de Recuperación recibían ketorolac 30 mg o morfina EV 1 – 3 mg pudiendo repetirse la dosis de esta última cada 15 min hasta que la Escala Verbal Numérica (0:sin dolor a 10:peor dolor imaginable) sea < o = 4. En la Unidad de Recuperación permanecían aproximadamente 1 hora y luego eran transferidos a la Unidad de Terapia Intensiva (UTI) donde se registró cada hora la tensión arterial, frecuencia cardíaca, frecuencia respiratoria, saturación de O2 y otros parámetros como diuresis, vómitos, drenajes, etc., por lo menos en las primeras 24 horas postoperatorias. Todos recibían O2 suplementario.
Se disponía de un anestesiólogo en el hospital de forma permanente, capaz de manejar las reacciones adversas de los opiodes y para registrar los datos pertinentes al trabajo.
Las reacciones adversas de la morfina IT incluyen:
- retención urinaria (que requieren sondaje vesical)
- prurito (sin importar la severidad)
- náuseas
- vómitos
- depresión respiratoria (FR < o = 10 por min.)
- sedación profunda ( sólo respuesta ante estímulos verbales o táctiles importantes)
- hipoxemia (oximetría < 90 %)
- las propias de la punción subaracnoides: cefalea postpunción dural, infecciones del LCR o SNC, lesión nerviosa, etc.
La analgesia en UTI se realizaba cuando el paciente manifestaba dolor, Escala Verbal Numérica (EVA) > o = 4 con morfina 3 mg ( pudiendo repetirse cada 15 min, ketorolac 30 o 60 mg o dextropropoxifeno más dipirona.
A las 24 y 36 hs un residente o staff de anestesiología registraba las dosis de analgésicos necesarios y las reacciones adversas de la morfina IT.
Resultados
Se estudiaron 37 pacientes sometidos a toracotomías que recibieron morfina IT como analgésico. La edad promedio fue de 50 ± 14,9 años . El 68 % era de sexo masculino. El 62% fue ASA II y el 38% ASA III. El peso fue de 73,7 ± 14,8 kg y la altura de 172 ± 77,5 cm (tabla 1).
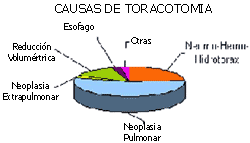
Las causas de las toracotomías fueron muy diversas (gráfico 1):
- Neoplasias pulmonares 56,8%
- Hidro – Neumo – Hemotórax 24,3%
- Reducción volumétrica (EPOC) 13,5%
- Neoplasias extrapulmonares 2,7 %
- Esófago 2,7 %
- Otras 2,7 %
La duración media del tiempo quirúrgico fue 207 ± 95,3 min. La necesidad de opiáceos EV durante la cirugía fue escasa, de tan sólo 117 ug de fentanilo en promedio por paciente. La extubación se pudo realizar en el 100% de los casos en la sala de cirugía.
La analgesia requerida por los pacientes fue mínima en unidad de recuperación, sin necesidad de analgésicos EV en el 72,9% de los pacientes. La misma tendencia se manifiesta la primeras 24 hs de UTI donde el 29,7% no requirió analgesia EV extra. En la mayoría de los que requirieron se usó ketorolac (14 ptes.) con un promedio de 59 mg por paciente. Tan solo 7 necesitaron opiodes EV (morfina o dextropropoxifeno + dipirona).
A partir de las 24 hs hasta las 36 hs evaluadas se requirió uso reglado de opiodes con AINES para calmar el dolor. Tan solo 1 paciente con toracotomía mínima fue dado de alta a las 36 hs sin necesidad de analgesia extra a la morfina IT.
La reacción adversa más frecuente fue la retención urinaria con el 67,6% ; pero en la población estudiada la mayoría eran hombres en una edad con alto índice de hiperplasia prostática benigna. Todos fueron manejados únicamente con sondeo vesical intermitente. Las náuseas se presentaron en un 38,8% con presencia de vómitos en un 18, 9%. Todos cedieron con la administración de antiheméticos de primera línea como la metroclopramida o domperidona.
El prurito, sin tener en cuenta la severidad fue del 29,7%, sin embargo los síntomas fueron manejados exitosamente con difenhidramina.
Las reacciones adversas más amenazantes como la depresión respiratoria y la sedación profunda se presentaron en el 2,7%. Fue un paciente de 45 años con el uso de 0,4 mg de morfina IT teniendo que usarse naloxona en unidad de recuperación para revertir el cuadro, sin presentar nunca hipoxemia.
Ningún paciente presentó cefalea postpunción dural, lesión nerviosa, infecciones, hematomas ni muerte.
Discusión
Un manejo apropiado del dolor es esencial después de una toracotomía. La razón no es sólo el intenso dolor, sino que el ineficaz control del dolor puede llevar a complicaciones pulmonares serias5. La expansion pulmonar inefectiva pueden predisponer a atelectasias, alteración en la relación ventilación/perfusión, hipoxemia e infección. El objetivo es proporcionar una analgesia eficaz para que los pacientes postoracotomías mantengan su capacidad residual funcional con inspiraciones profundas, expulsión de secreciones con la tos y temprana movilización para una precoz recuperación y acortar la estadía hospitalaria 6.
Una buena alternativa para lograr los objetivos con una técnica de bajo costo, sencilla, eficaz y confiable es la utilización de morfina IT, siempre suplementada con analgésicos EV para proveer una mejor analgesia.
La administración de morfina IT produce una intensa y prolongada analgesia con un comienzo de acción de entre 15 – 45 minutos y una duración de entre 18 y 24 horas7.
Originalmente se emplearon grandes dosis de morfina de entre 2-15 mg 8 y si bien la analgesia obtenida fue de mayor duración, la incidencia de reacciones adversas también lo fue.
Aunque en los años siguientes a su introducción la técnica demostró su efectividad, su uso fue limitado comparado con la analgesia peridural, debido a la percepción que esta vía está asociada a un mayor número de reacciones adversas, incluyendo la depresión respiratoria tardía, la cual estuvo relacionada al hacer el análisis retrospectivo con la alta dosis de morfina empleadas.
Uno de los limitantes del alivio del dolor de la morfina es la duración que en nuestro trabajo fue de 25 ± 6,5 hs en comparación con la epidural contínua.
En cuanto a la dosis recomendada de morfina intratecal para toracotomía existen diferentes opiniones en la literatura, Gray et al en 19869 empleó dosis de 10 mcg/kg (0.5-1.2 mg como dosis total), Cohen et al en 1993 10 utilizó dosis de 12 mcg/kg, Gwirtz et al en 1999 4utilizo entre 0.65 y 0.8 mg como dosis total y en publicaciones más recientes se emplearon dosis de 0.5 mg de morfina con 50 mcg de sufentanil con excelentes resultados 11.
En nuestro trabajo utilizamos Morfina intratecal en dosis bajas, la dosis total osciló entre 0.3 y 0.8 mg, administrando las dosis más bajas a pacientes mayores de 65 años de edad, con mal estado general y en aquellos con mala función pulmonar preoperatoria, en quienes se ha observado mayor incidencia de depresión respiratoria en investigaciones como la de Gjessing y Tomlin 7, o la de Gray et al. 9.
Para la dilución de la morfina usamos solución fisiológica en un volumen de 1.5 a 4 ml. Trabajos como el de Gray y Glenn demostraron menor duración de la analgesia cuando se realizó la dilución en dextrosa al 5 o 10% debido a un enlentecimiento en la diseminación de la morfina a trvés del LCR hacia los segmentos torácicos, ocupando mayor número de receptores en la región lumbosacra (cerca del sitio de inyección), con el consiguiente déficit de analgesia en los segmentos más altos .
La reacción adversa más temida es la depresión respiratoria la cual se presentó en un solo paciente, 2,7%, porcentaje similar a la serie de 5969 casos presentado por Indiana University Hospital (3%) para diferentes tipos de cirugías. Ésta fue de fácil reversión con naloxona, sin presentarse ninguna catástrofe respiratoria, muerte o intubación endotraqueal de emergencia. Ningún paciente presentó hipoxemia, medida por saturación de O2, aunque todos recibieron O2 suplementario.
La depresión respiratoria que sigue a la administración de opiodes epidurales / intratecales ocurre a dos diferentes intervalos 12,13.
La depresión respiratoria temprana ocurre dentro de las dos primeras horas de la inyección del opiode, generalmente es secundaria al uso de opiodes lipofílicos del tipo del fentanilo y sufentanilo inyectados por vía peridural y resultaría de la rápida absorción sistémica y es de similar magnitud a la observada luego de opiodes parenterales. Cararcterísticamente se produce en forma rápida y generalmente es de menor importancia clínica que la depresión respiratoria tardía y más probablemente ocurra en los lugares altamente controlados, como en el quirófano o en la sala de recuperación con el anestesiólogo presente o inmediatamente disponible.
La depresión respiratoria tardía resulta de la migración cefálica del opiodes (generalmente morfina) dentro del líquido cefaloraquídeo y su subsecuente interacción con los receptores opiodes del centro respiratorio del bulbo raquídeo, su inicio es variable, pero generalmente es evidente 6 a 10 horas siguientes a la administración intratecal o peridural de la morfina y puede persistir hasta 24 horas.
Clásicamente se desarrolla en forma lenta y progresiva, generalmente precedida de náuseas y vómitos y un incremento de la sedación, su signo clínico más confiable es una depresión del nivel de conciencia (incremento de la somnolencia) posiblemente causado por la hipercarbia 12,14,15.
La reacción adversa más frecuente fue la retención urinaria con el 67,6% a pesar de que el 10,8% de los pacientes tenían sonda vesical para medición de diuresis contínua. Esto se puede explicar por los siguientes factores relacionados: gran porcentaje de hombres, cuya edad media es compatible con el desarrollo de hiperplasia prostática benigna y el uso de opiodes EV.
Las otras reacciones que se presentaron: náuseas (38,8%), vómitos (18,9%), prurito (29,7%), a pesar de manifestarse en un número importante de casos , todos cedieron con los tratamientos convencionales (metroclopramida, domperidona, difenhidramina).
No se presentaron casos de cefalea postpunción dural, diversos factores pueden explicarlo: los pacientes permanecieron en posición supina en el postoperatorio, las agujas eran todas punta de lápiz y de diámetro muy pequeño (27 G), los pacientes eran mayores de edad y de sexo masculino en su mayoría y también por el bajo número de pacientes estudiados.
El requerimiento de analgésicos como suplemento a la morfina IT fue escaso tanto en el intraoperatorio (el promedio de fentanilo utilizado fue de 117 ug/paciente) como en el postoperatorio, sin requerir analgésicos en recuperación el 72,9%y en las primeras 24 hs el 29,7% de los pacientes. Existe un claro incremento en el riesgo de desarrollar depresión respiratoria por el uso suplementario de opioides EV durante las primeras 24 horas del postoperatorio, utilizamos antiinflamatorios (Ketorolac 30 mg) en los pacientes que refirieron dolor durante este período 16,17, en la mayoría de los casos. Aunque se podría haber sido más agresivo en la analgesia EV, sobretodo cuando los pacientes realizan terapia respiratoria a los que se les puede dejar reglados analgésicos preventivos antes de la terapia respiratoria o idealmente con Analgesia Controlada por el Paciente (PCA).
Cohen y Neustein en 1993 demostraron una reducción significativa en los requerimiento de Enflurano en cirugía cardíaca 60 minutos después de la inyección preoperatoria de 12 ug/kg de morfina intratecal 18. Si bien nuestro trabajo es de observación clínica, y no contamos con un grupo control, hemos comprobado que la concentración necesaria de anestésicos inhalatorios para el mantenimiento de la anestesia general fue relativamente baja; entre 1,5 y 2% para Isofluorano, 1 a 1.5% para Halotano y 2 a 4% para sevofluorano, que fueron los agentes utilizados.
En la sala de recuperación objetivamos en coincidencia con muchos reportes, que los pacientes estaban tranquilos y lúcidos en su gran mayoría, que eran capaces de respirar normalmente, toser y realizar inspiraciones profundas si se les solicitaba.
Otro beneficio de la vía intratecal es la reducción de costos. En el estudio de costos del Indiana University Hospital con 5969 casos refiere que el costo de los opiodes intratecales es menor a un tercio que el de opiodes epidurales para analgesia postoperatoria4.
Es muy importante la educación y el entrenamiento aportados al servicio de enfermería, con el uso de protocolos claros y sencillos para monitorear y detectar las reacciones adversas. Contando con anestesiólogo de guardia en el hospital para actuar en situaciones cruciales por la seguridad del paciente. Concientizando al médico anestesiólogo de guardia a responder al servicio de enfermería de forma rápida, razonable y creíble para alentar la comunicación entre ambos como nexo con el paciente4.
Por lo tanto creemos que la analgesia con morfina IT para el manejo del dolor postoperatorio de las toracotomías es una alternativa segura, eficaz y económica para el manejo rutinario del dolor agudo postoperatorio de las primeras 24 hs, coadyuvada por opiodes o Aines EV; si se dispone de protocolos estrictos, personal de enfermería entrenado y anestesiólogo en el establecimiento las 24 hs, para la seguridad y bienestar del paciente.
| Tabla 1 Datos Demográficos |
|
| Edad (años) |
50 ± 14.9 |
| Sexo M/F | 25/12 |
| Peso (Kg) | 73.7 ± 14.8 |
| Altura (cm) | 172 ± 77.5 |
| ASA II | 62 % |
| ASA III | 38 % |
 [ Ampliar imagen ] |
| Gráfico 1 |
| Tabla 2 Reacciones adversas |
|
| Retención urinaria | 67,6 % |
| Nauseas | 38,8 % |
| Prurito | 29,7 % |
| Vómitos | 18,9 % |
| Depresión respiratoria | 2,7 % |
| Sedación profunda | 2,7 % |
| CPPD | 0 % |
| Lesión nerviosa | 0 % |
| Infecciones | 0 % |
| Muerte | 0 % |
Bibliografía
- Mason N, Gondret R, Junca A, Bonnet F. Intrathecal sufentanil and morphine for post-thoracotomy pain relief. Br J Anaesth 2001; 86: 236-240
- Behar M, Olswang D, Magora F et al. Epidural morphine in the treatment of pain. Lancet 1979;1:527-9
- Wang JK, Nauss LA, Thomas JE. Pain relief by intrathecally applied morphine in man. Anesthesiology 1979; 50:149-51
- Gwirtz KH, Young JV, Byers RS, Alley C, Levin K, Walker SG, Stoelting RK The safety and efficacy of intrathecal opioid analgesia for acute postoperative pain: seven year's experience with 5969 surgical patients at Indiana University Hospital. Anesth Analg 1999;88:599-604
- Peeters-Asdourian C, Guta S; Choices in Pain Management Following Thoracotomy; Chest 1999,115,S 122S-124S
- Soto RG,Fu ES; Acute Pain Mnagement for Patients Undergoing Thoracotomy; Ann Thorac Surg 2003; 75:1349-57
- Gjessing J., Tomlin P.J. Postoperative pain control with intrathecal Morphine. Anaesth 1981; 36: 268- 76.
- Samii K, Chauvin M, Viars P. Postoperative spinal analgesia with morphine Br J Anaesth 1981; 53: 817-820
- Gray JR, Fromme GA, Nauss LA. Intrathecal morphine for post-thoracotomy pain. Anesth Analg 1986; 65: 873-876
- Cohen E, Neustein SM. Intrathecal morphine during thoracotomy, Part I J Cardiothorac Vasc Anesth 1993; 7:154-156
- Liu N, Kuhlman G, Dalibon N, Moutafis M, Levron JC. A randomized, double-blinded comparison of intrathecal morphine, sufentanil and their combination versus IV morphine PCA for post-thoracotomy pain. Anesth Analg 2001; 92:31-36
- Etches RC, Sandler A, Daley MD. Respiratory depression and spinal opioids Can J Anaesth 1989; 36: 165-185
- Kafer ER, Brown J, Scott D, et al. Bifasic depression of ventilatory responses to CO2 following epidural morphine. Anesthesiology 1983;58:418
- Ready LB, Loper KA, Nessly M, Wild L. Postoperative epidural morphine is safe on surgical wards. Anesthesiology 1991; 75:452-456
- Ready LB, Oden R, Chadwick HS, et al. Development of an anesthesiology- based postoperative pain management service. Anesthesiology 1988;68:100-106
- Vaughan RS. Pain relief after thoracotomy. Br J Anaesth 2001; 87: 681-683
- Rawal N, Arner S, Gustafsson L, Allvin R Present state of extradural and intratecal opioid analgesia in Sweden. Br J Anaesth 1987; 59:791-799
- Cohen E. MD, Neustein S. MD. Intrathecal Morphine during Thoracotomy, Part I: Effect on intraoperative Enflurane requirements. Journal of Cardiothoracic and Vascular Anesthesia, Vol 7, n° 2 (April), 1993: 154- 6.
- Loan WB, Morrison JD. The incidente and severity of postoperative pain.Br. J Anaesth 1967;39:695-698
- Kavanagh BP, Katz J, Sandler AN. Pain control after thoracic surgery. Anesthesiology 1994; 81: 737-759
- Stoelting RK. Intrathecal morphine: an underused combination for postoperative pain management. Anesth Analg 1989;68:707-9
- Conacher ID. Pain relief after thoracotomy. Br J Anaesth 1990;65:806-812
- Kavanagh BP, Katz J, Sandler AN. Pain control after thoracic surgery Anesthesiology 1994; 81:737-759
- Perttunen K, Nilsson E, Kalso E. I.v. diclofenac and ketorolac for pain after thorascopic surgery Br J Anaesth 1999; 82:221-227
- Shahnaz CA. Perioperative pain management in patients undergoing thoracic surgery. Curr Opin Anaesthesiol 2001; 14:87-91
- Kavanagh BP, Azad SC, Groh J, Beyer A, et al. Continuous epidural analgesia vs patient control intravenous analgesia for post-thoracotomy pain. Acute Pain 2000; 3:84-93
- Mahon SV, Berry PD, Jackson M, et al . Thoracic epidural infusions for post-thoracotomy pain: a comparison of fentanyl-bupivacaine mixtures vs fentanyl alone. Anaesthesia 1999; 54: 641-646
- Neustein SM, Cohen E. Intrathecal morphine during thoracotomy, Part II J Cardiothorac Vasc Anesth 1993; 7: 157-159
- Mason NP, Bonnet F, Vaughan RS. Pain relief after thoracotomy (correspondence) Br J Anaesth 2002; 88: 880-881
- Chaney MA, Side effects of intrathecal and epidural opioids (review article) Can J Anaesth 1995; 42: 891-902
- Morgan M. The rational use of intrathecal and extradural opioids Br J Anaesth 1989; 63: 165-188
- Jordan C. Assessment of the effects of drugs in respiration. Br J Anaesth 1982; 54: 763-782
- Fuller JG, McMorland GH, Douglas MJ, Palmer L. Epidural morphine for analgesia after caesarean section: a report of 4880 patients. Can J Anaesth 1990; 37:636-640
- Gustafsson LL, Schildt B, Jacobsen K. Adverse effects of extradural and intrathecal opioids: report of a nationwide survey in Sweden. Br J Anaesth 1982; 54: 479-486
- Loper KA, Ready LB. Epidural morphine after anterior cruciate ligament repair: a comparison with PCA morphine. Anesth Analg 1989; 68:350
- Chadwick HS, Ready LB. Intrathecal and epidural morphine sulfate for postcesarean analgesia: a clinical comparison. Anesthesiology 1988; 68:925-929
- Tuman K.J., Mc Carthy R.J., March R.J., et al. Effects of epidural anesthesia and analgesia on coagulation and outcome after vascular surgery. Anesth Analg 1991; 73: 696- 704.
- Yeager M.P., Glass D.D., Neff R.K., Brinck-Johnsen T. Epidural anesthesia and analgesia in high- risk surgical patients. Anesthesiology 1987; 66: 729- 36.
- Gjessing J., Tomlin P.J. Postoperative pain control with intrathecal Morphine. Anaesth 1981; 36: 268- 76.
- Gray J.R., Fromme G.A., Nauss L.A., Wang J.K. Intrathecal Morphine for post-thoracotomy pain. Anesth Analg 1986; 65: 873- 6.
- Cousins M.J. MD, F.F.A.R.A.C.S.; Mather L.E. PhD. Intrthecal and Epidural administration of opioids. Anesthesiology, Sep 1984, Vol 61, n° 3: 276- 310.
- Chaney, MD. Side effects of intrathecal and epidural opioids. Canadian Journal of Anaesthesia, October 1995, vol 42, n° 10.
- Bromage P.R., MB, BS, F.F.A.R.C.S. The price of intraspinal narcotic analgesia: basic constraints. Anesth Analg. July 1981, Vol 60, n° 7.
- Odoom J. MD, Sih I. MD. Respiratory depression after intrathecal Morphine. Letters to the editor. Anesth Analg, January 1982, Vol 61, n° 1.
- Ready L.B., Oden R., Chadwick H.S., et al. Development of an anesthesiology- based postoperative pain management service. Anesthesiology, 1988; 68: 100- 6.
- Goodman Gilman. 10° Edition, 2001. Opioids Analgesics. Chapter 23: 569- 75.
- Bailey P. MD, Rhondeau S. MD, et al. Dose- response pharmacology of intrathecal Morphine in human volunteers. Anesthesiology, Jul 1993, Vol 79, n° 1.
- Miller R. 4° Edición, 1998. Cap. 12: 284- 89.
- Davies G.K., Tolhurst- Cleaver C.L., James T.L. Respiratory depression after intrathecal narcotics. Anaesthesia, 1980, Vol 35: 1080- 83.
- Jones M., F.F.A.R.A.C.S. et al. Intrathecal Morphine: Naloxone reverses respiratory depression but not analgesia. British Medical Journal. Short reports, vol 281, 6, Sep 1980.